فهرست مطالب
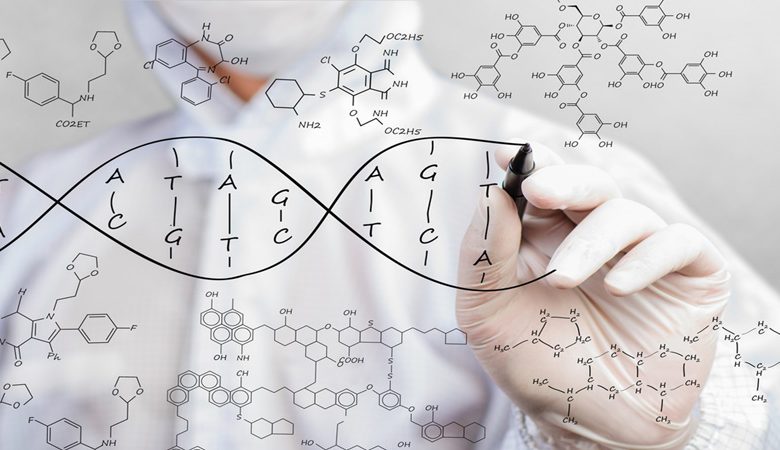
ژنتیک مولکولی (molecular genetics) ، شاخهای از زیستشناسی است که به بررسی نحوه بیان ژن، ساختار و عملکرد آنها میپردازد. با مطالعه ژنتیک انواع موجودات و ارگانیسمها، میتوان درک شفاف و روشنی از متابولیسمهای مختلف آنها و همچنین بیماریها و کارکرد سلولها بدست آورد. مطالعه مبانی ژنتیک مولکولی، به ما کمک میکند تا بتوانیم زیستشناسی تکاملی و تغییرات به وجود آمده در ساختار ژنها را طی زمان، بهتر درک کنیم.
ژنتیک مولکولی از دیدگاه بیولوژی
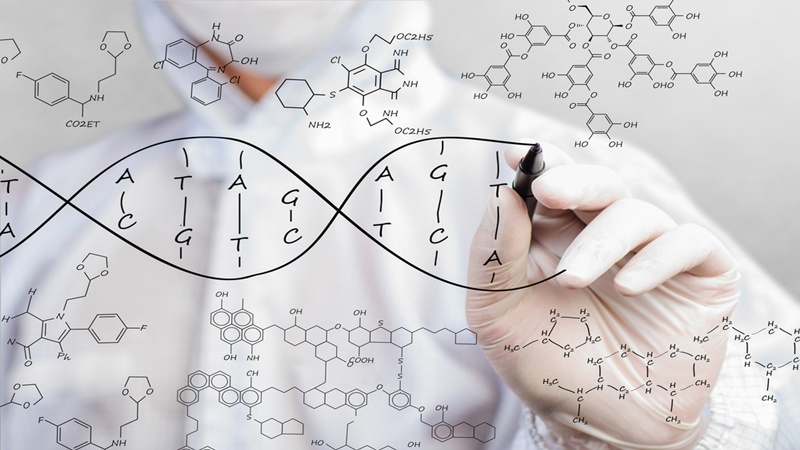
ژنتیک مولکولی از دیدگاههای مختلفی در علم بیولوژی بررسی میشود که هر کدام، مفهوم خاصی را دنبال میکنند. “نظریهی بنیادی” در molecular genetics، اذعان میکند که ژنها، با تولید پلیپپتیدهای متنوع فرایندهای درون سلولی و برون سلولی را هدایت میکنند. “نظریه پایه” دیگری نیز وجود دارد که این مفهوم را به بیان و تنظیم ژنها در سطح مولکولی توصیف میکند. همچنین اگر بخواهیم از دیدگاه “زیستشناسی پزشکی” به آن نگاه کنیم، ژنتیک مولکولی رویکردی تحقیقی در درمان و پیشگیری از بیماریها خواهد بود.
اصطلاح ژنتیک مولکولی که توسط برخی از محققان مطرح میشود، در واقع همان “ژنتیک معاصر” است. چرا که علم ژنتیک، از دو بخش مولکولی و غیرمولکولی تشکیل نشدهاست و ژنتیک معاصر، مفهوم کلی این علم را عنوان میکند. ژنتیک مولکولی با “رویکرد تحقیقی” با به کار بردن تکنیکهای ژنتیک مولکولی، پیرو دانش اولیه در مورد بیان و تنظیم ژنها در سطح مولکولی، در زیستشناسی پزشکی کاربرد دارد. همچنین باید اشاره نمود که “نظریه اساسی ژنتیک کلاسیک” در مورد ساختار، بیان و تنظیم ژنها و نحوه وراثت صفات و ژنها به نسل بعدی مطالعه میکند.
تاریخچه ژنتیک مولکولی، از گذشته تا به امروز
زیستشناسی مولکولی برای اولین بار در دهههای 1930 و 40 سرچشمه گرفت و آن را به یک رشته علمی نسبتاً جدید تبدیل کرد. وارن ویور، مدیر بخش علوم طبیعی در بنیاد راکفلر، در سال 1938 در گزارشی برای بنیاد، اصطلاح “زیستشناسی مولکولی” را مطرح کرد. این گزارش، از مطالعهای برخواسته از تحول ژنتیکی در باکتریها، بود و سرآغاز molecular genetics شد.
در خلال سالهای 1945 تا 1970، ماکس لودویگ هنینگ دلبروک، با کمک دیگر محققان در “گروه فاژ” توانستند، اطلاعات بالقوهای را در خصوص ژن، کدونها و در بیان کلی ژنتیک مولکولی ارائه دهند. سرآغاز دوره کلاسیک زیستشناسی مولکولی را میتوان به کشف ساختار مارپیچ دوگانه DNA، توسط جیمز واتسون و فرانسیس کریک در سال 1953، نسبت داد. پس از آن، یک مطالعه قابلتوجه توسط سیدنی برنر و همکارانش، انجام شد که در نتیجه “فرضیه توالی” را مطرح نمود.
در خلال سال 1972 بود که کوهن و بویر، با مطالعات پژوهشی خود توانستند بنای شبیهسازی مولکولی را پیریزی کنند و اطلاعات سودمندی را برای آینده فراهم کنند. در آیندهی نه چندان دور، تکنیکهای توالییابی توسط گیلبرت و سپس توسط فردریک سنگر روی کار آمد تا آغازی باشد برای غربالگریهای ژنتیکی در سال 1985. در حدود یک دهه از این پژوهش سنگر نگذشته بود که در پروژه توالییابی ژنوم انسان که یک پروژه بینالمللی بود، توالییابی شد. این، پایان ماجرا نبود و تا به الان، تحقیقات گستردهای در خصوص علم ژنتیک مولکولی در جریان است و یافتههای ارزشمندی کشف شدهاست.
مبانی ژنتیک مولکولی
مفاهیم پایه و اساسی ژنتیک یا به بیان بهتر، مبانی ژنتیک مولکولی شامل مباحثی میشود که ساختار و تمام مکانیسمهای مرتبط با ژنها را در بر بگیرد. بنابراین تعریف تمام مفاهیم در خصوص ساختار ژنها، همانندسازی، رونویسی، ترجمه، ترمیم، سیگنالینگ، تنوع ژنتیکی، جهشها و تغییرات مهم در ساختار ژنها و…، جزئی از مبانی ژنتیک مولکولی هستند. مطالعه درباره این مفاهیم، از اهمیت بالایی برخوردار است؛ زیرا هر گونه تغییر در آنها که موجب عملکرد نامناسب ژنها شود، میتواند در متابولیسمها و فنوتیپ یک ارگانیسم، تاثیرگذار باشد.
بیماریهای ژنتیکی با هر دلیل محیطی و یا اپیژنتیکی که ایجاد شده باشند، درنهایت موجب تغییر در ساختار یک ژن و یا محصول نهایی آنها میشود. از اینرو، دانش ما از مبانی ژنتیک مولکولی کمک میکند تا بتوانیم از طریق تکنیکهای ژنتیک مولکولی به درمان و یا پیشگیری از این بیماریها کمک کنیم. ساختار ژنها و مکانیسمهای مختلف مرتبط با آنها، دنیای بسیار پیچیده و گستردهای دارد و شاید هنوز هم درک ما از آنها کامل و شفاف نباشد. با مطالعه این مفاهیم، میتوان با استفاده از تکنیکهای ژنتیک مولکولی بسیاری از بیماریها را درمان کرد، بیان ژنهای خاصی را خاموش کرد و در حیطه زیستشناسی پزشکی دستاوردهای بسیاری داشت.
دانش مبانی ژنتیک مولکولی به ما کمک میکند تا بتوانیم علت بسیاری از صفات را بدانیم، تکامل را بهتر درک کنیم و هدفمندتر در حیطه ژنتیک مولکولی گام برداریم.
تکنیکهای ژنتیک مولکولی

همانطور که میدانید فقط زمانی میتوانیم به شناخت بیشتر ژنها دست پیدا کنیم که با کمک تکنیکهای ژنتیک مولکولی به بررسی و تحقیق در مورد آنها بپردازیم. بنابراین، با مطالعه ژنومی افراد میتوان علت انواع مختلفی از بیماریها را شناخت، نسبت به پیشگیری و درمان بیماریها اقدام نمود و جمعیتها را از نظر فنوتیپهای مختلف بررسی کرد. molecular genetics lab techniques یا تکنیکهای آزمایشگاهی ژنتیک مولکولی، بسیار متنوع هستند و در ادوار گذشته پیشرفتهای چشمگیری داشتهاند. در این جا، به برخی از رایجترین روشهای آزمایشگاهی ژنتیکی اشاره خواهیم کرد.
● PCR
واکنش زنجیرهای پلیمراز (PCR)، روشی برای تکثیر DNA است که در یک لوله آزمایش (یعنی در شرایط آزمایشگاهی) انجام میشود. در این روش، “پلی مراز” به آنزیم DNA پلیمراز استخراجشده و خالصشده از باکتریها اشاره دارد. “واکنش زنجیرهای” نیز به توانایی این تکنیک اشاره دارد که میلیونها نسخه از یک مولکول DNA را تولید میکند. این کار، با استفاده از هر مارپیچ دوتایی که به تازگی تکرار شدهاست بهعنوان یک الگو برای سنتز دو مولکول انجام میشود. بنابراین PCR، یک روش بسیار کارآمد برای افزایش DNA است.
● استخراج RNA
هدف از استخراج RNA، به دست آوردن RNA خالصشده با کیفیت بالا از نمونههای بیولوژیکی برای کاربردهایی مانند توالییابی، آنالیز رونوشت و آزمایش پاتوژن عفونی است. بهطور گسترده، سه تکنیک اصلی برای استخراج RNA استفاده میشود: استخراج آلی مانند محلولهای مبتنیبر فنل-گوانیدین ایزوتیوسیانات (GITC)، فناوری ستون چرخشی مبتنیبر غشای سیلیسی و فناوری ذرات پارامغناطیسی. یکی از متداولترین روشهای مورد استفاده، استخراج آلی مبتنیبر فنل-GITC است.
● استخراج DNA
استخراج DNA، روشی برای خالصسازی DNA با استفاده از روشهای فیزیکی و یا شیمیایی از نمونه جداسازیشده DNA از غشای سلولی، پروتئینها و سایر اجزای سلولی است. فردریش میشر در سال 1869، برای اولین بار جداسازی DNA را انجام داد. استخراج DNA، شامل لیز کردن سلولها و حل شدن DNA است که با روشهای شیمیایی یا آنزیمی، برای حذف ماکرومولکولها، لیپیدها، RNA یا پروتئینها انجام میشود.
● تخلیص DNA
استراتژیهای خالصسازی DNA، بر ویژگیهای شیمیایی DNA متکی است که آن را از سایر مولکولهای سلول متمایز میکند. برای استخراج DNA خالصشده از یک نمونه بافت، سلولها را با آسیاب کردن یا لیز کردن در محلولی که حاوی مواد شیمیایی است باز میکنند. این محلول، از DNA محافظت میکند و در عین حال، سایر اجزای سلول را تخریب میکند. این مواد شیمیایی، ممکن است شامل شویندههایی باشد که غشاهای لیپیدی را حل میکنند و پروتئینها را تغییر میدهند.
● تکثیر DNA با پلاسمید
بسیاری از باکتریها، حاوی عناصر DNA خارج کروموزومی بهنام پلاسمید هستند. پلاسمیدها، معمولاً مولکولهای کوچک (چند 1000 جفت باز)، دایرهای و دو رشتهای هستند که مستقل از کروموزوم تکثیر میشوند. پلاسمیدها، میتوانند در تعداد کپیهای بالایی در یک سلول وجود داشته باشند. پلاسمیدها اغلب حامل ژنهایی برای بیماریزایی و مقاومت دارویی هستند.
● ARMS PCR
Amplification Refractory Mutation System PCR (ARMS-PCR)، یکی از دقیقترین تکنیکهای ژنتیک مولکولی در تشخیص بیماریهای ژنتیکی در روزهای اخیر است. این تکنیک، یک روش استاندارد طلایی، برای تالاسمی و کم خونی داسی نیز به شمار میرود. علاوه بر این، در تشخیص جهش JAK2 و HIV نیز قابل استفاده است. ARMS-PCR، میتواند برای تعیین SNPها برای تشخیص جهش در پانلهای مختلف بیماری استفاده شود.
● Nested PCR
Nested PCR، معمولاً شامل دو واکنش افزایشی متوالی است که هر کدام از یک جفت پرایمر متفاوت استفاده میکنند. محصول اولین واکنش، بهعنوان الگوی PCR واکنش دوم استفاده میشود که توسط اولیگونوکلئوتیدهایی که در داخل جفت پرایمر اول قرار میگیرند، آغاز میشود.
● ژل الکتروفورز عمودی و افقی
محلول DNA بی رنگ است و به جز چسبناک بودن در غلظتهای بالا، از نظر بصری نیز از آب قابل تشخیص نیست. بنابراین، تکنیکهایی مانند الکتروفورز ژل برای تشخیص و تجزیه و تحلیل DNA، توسعه یافته است.
● سنتز Cdna
سنتز cDNA، تولید DNA مکمل (cDNA) از یک الگوی RNA با رونویسی معکوس است. ترانس کریپتازهای معکوس (RTs) از یک الگوی RNA و یک پرایمر مکمل RNA، برای هدایت سنتز اولین رشته cDNA استفاده میکنند. این رشته میتواند مستقیماً بهعنوان یک الگو برای واکنش زنجیرهای پلیمراز (PCR) استفاده شود. این ترکیب رونویسی معکوس و PCR (RT-PCR)، امکان تشخیص RNAهایی با فراوانی کم در یک نمونه و تولید cDNA مربوطه را فراهم میکند و در نتیجه، شبیهسازی ژنهای کم کپی را تسهیل میکند.
● RFLP PCR
تفاوت در توالیهای DNA همولوگ را میتوان با حضور قطعات با طولهای مختلف، پس از هضم نمونههای DNA موردنظر با کمک اندونوکلئازهای محدودکننده خاص تشخیص داد. هدفRFLP این است که هر DNA ژنومی را میتواند براساس وجود یا عدم وجود مکانهای آنزیم محدودکننده، تمایز دهد.
● بلاتینگ و هیبریدیزاسیون
نوارهای DNA در یک ژل الکتروفورتیک، تنها در صورتی تشکیل میشوند که اکثر مولکولهای DNA، به یک اندازه باشند، مانند واکنش PCR یا restriction digestion of a plasmid. در شرایط دیگر، بهعنوان مثال پس از هضم محدود DNA کروموزومی (ژنومی)، تعداد زیادی قطعه، با اندازه متغیر، در هضم وجود خواهد داشت و به جای نوارهای مجزا، بهصورت یک اسمیر پیوسته از DNA ظاهر میشود.
ژن درمانی
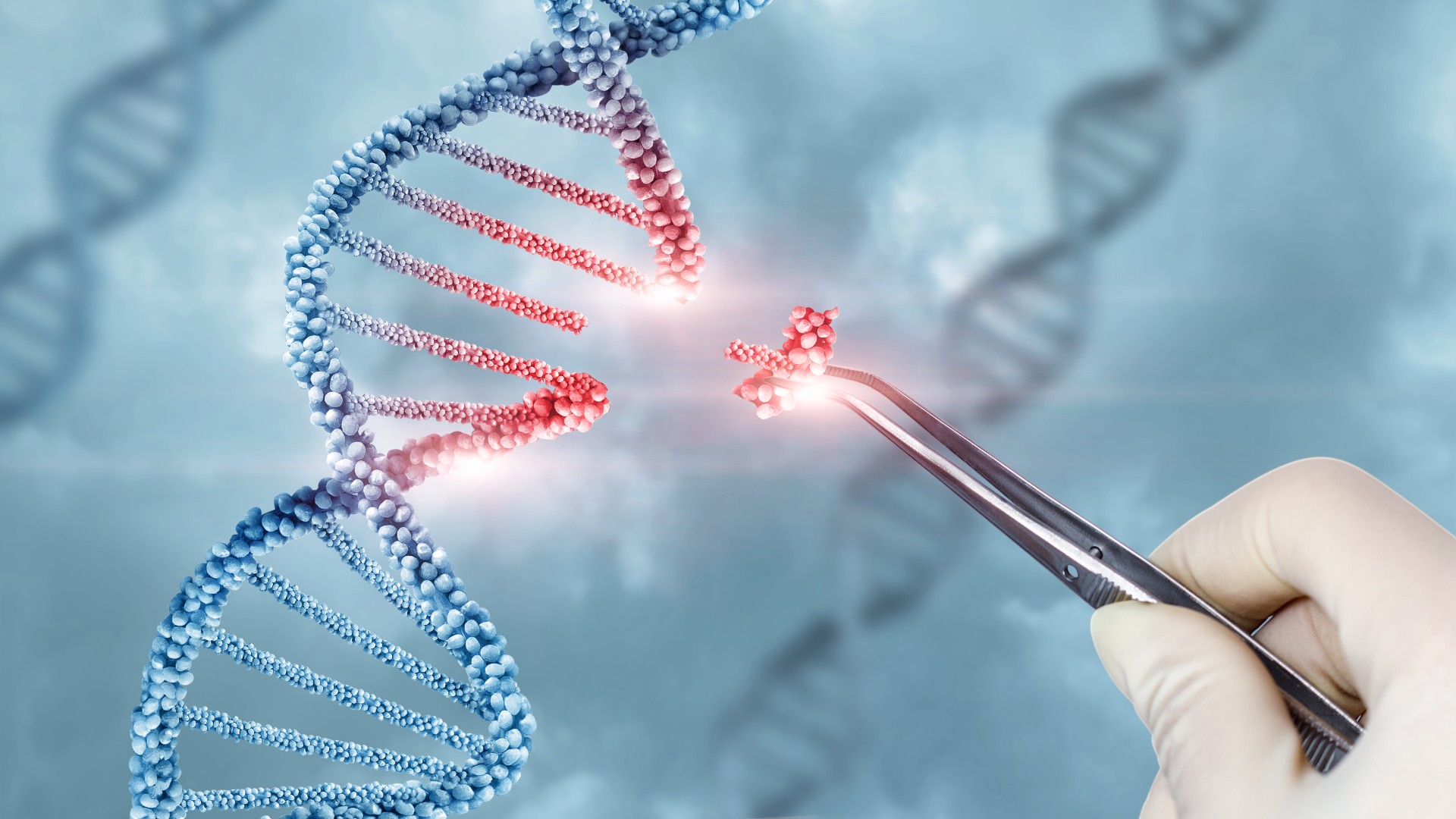
ژن درمانی، یکی از روشهای نوین درمان بیماریهای ژنتیکی با کمک اصلاح ژنهای معیوب و ناقص است که در سالهای گذشته، پیشرفت چشمگیری داشته است. تکنیکهای ژن درمانی به پزشکان این امکان را میدهد که به جای استفاده از دارو یا جراحی، با تغییر ساختار ژنتیکی یک اختلال را درمان کنند. اولین روش ژن درمانی که اغلب انتقال ژن یا افزودن ژن نامیده میشود. به منظور معرفی یک ژن جدید به سلولها برای کمک به مبارزه با یک بیماری توسعه داده شد. اساساً سه نوع ژن درمانی وجود دارد: ex vivo، in vivo و in situ.
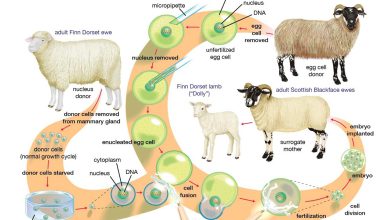
در ژن درمانی ex vivo، سلولهای هدف، از بدن بیمار خارج میشوند، که با کمک ژن درمانی یا سایر دستکاریهای ژنتیکی که امکان اصلاح فنوتیپ بیماری را فراهم میکند، مهندسی شدهاند. ژن درمانی In vivo به تحویل مستقیم مواد ژنتیکی بهصورت داخل وریدی یا بهصورت موضعی (in situ)، به یک عضو خاص (مثلاً مستقیماً در چشم) گفته میشود. ژن درمانیin vivo با کمک یک ناقل که بهطور مستقیم نسخههای عملکردی یک ژن را به سلولهای هدف وارد میکند تا یک ژن جهشیافته یا گمشده را درمان کند، کار میکند. در حال حاضر، برخی از ژن درمانیهای تاییدشده مواد ژنتیکی را در داخل بدن ارائه میکنند.
جامعترین دورهی ژندرمانی برای نخستین بار در کشور
سخن پایانی
ژنتیک مولکولی یا به بیان بهتر، ژنتیک معاصر، علمی بسیار کاربردی در زیستشناسی پزشکی است که پس از توالییابی کل ژنوم انسان، هر ساله پیشرفت چشمگیری داشته است. با دانستن و به کار بردن مبانی ژنتیک مولکولی، میتوان نسبت به علت انواع مختلفی از بیماریها، فنوتیپها، اطلاعات پرباری بدست آورد.
نویسنده و ویراستار: زینب رضائی
منابع:
- https://plato.stanford.edu/entries/molecular-genetics/
- https://bio.libretexts.org/
- https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6425773/#:~:text=DNA%20extraction%20is%20a%20method,proteins%2C%20and%20other%20cellular%20components.
- https://bmcresnotes.biomedcentral.com/articles/10.1186/1756-0500-4-3#:~:text=There%20are%20three%20major%20techniques,%2DGITC%2Dbased%20organic%20extraction.
- https://www.cd-genomics.com/diseasepanel/arms-pcr-in-disease-research.html#:~:text=The%20Amplification%20Refractory%20Mutation%20System,thalassemia%20and%20sickle%20cell%20anemia.
- https://pubmed.ncbi.nlm.nih.gov/30710024/#:~:text=Nested%20PCR%20usually%20involves%20two,to%20the%20first%20primer%20pair.
- https://www.ncbi.nlm.nih.gov/probe/docs/techrflp/
- https://international.neb.com/applications/dna-amplification-pcr-and-qpcr/rt-pcr-and-cdna-synthesis/cdna-synthesis#:~:text=cDNA%20Synthesis%20describes%20the%20generation,RNA%20template%20by%20reverse%20transcription.
2 نظرها