فهرست مطالب
شاید برایتان جالب باشد از تاریخچه ژندرمانی و پیشرفت آن در 10سال اخیر بدانید، آیا پیشرفتی داشته است یا …؟ باید بگوییم امروزه ژندرمانی، یک حوزه داغ در صنعت بیوتکنولوژی بهشمار میرود. با وجود تمامی فرازونشیبهایی که ژندرمانی در مسیر تکاملی خود داشته، در طول چند سال گذشته شاهد جریان تقریبا ثابتی از اخبار مثبت درخصوص موفقیتهای ژندرمانی بودهایم. همچنین مبالغ هنگفتی برای توسعه این روش درمانی جمعآوری شده و با بیش از 1000 کارآزمایی بالینی که در حال انجام است، امیدواریم شاهد ورود طولانیمدت انقلاب ژندرمانی باشیم. با ما همراه باشید تا در این مطلب به تاریخچه ژندرمانی در حدود 10سال اخیر بپردازیم.
قبل از بیان تاریخچه ژندرمانی باید سری بزنیم به مفاهیم آن پس در ابتدا باید بگوییم؛ مفاهیم ژندرمانی ابتدا در طول دهه 1960 و اوایل 1970، در حالی که توسعه خطوط سلولی مشخصشده ژنتیکی و شفافسازی مکانیسمهای تبدیل سلولی توسط «پاپاواویروسهای پلیوما» و «SV40» در حال پیشرفت بود، مطرح شد. با ورود تکنیکهای DNA نوترکیب، ژنهای شبیهسازی شده در دسترس قرار گرفتند و برای نشاندادن اینکه ژنهای خارجی میتوانند نقصهای ژنتیکی و فنوتیپهای بیماری را در سلولهای پستانداران در شرایط آزمایشگاهی تصحیح کنند، مورد استفاده قرار گرفتند. ناقلهای رتروویروسی کارآمد و سایر روشهای انتقال ژن، نمایش متقاعدکنندهای از تصحیح فنوتیپ کارآمد در شرایط آزمایشگاهی را امکانپذیر کردهاند. اکنون ژندرمانی به یک رویکرد پذیرفتهشده برای درمان تبدیل کرده و مطالعات کاربردی بالینی را با بیماران انسانی توجیه میکند.
اولین تأییدیههای ژندرمانی
چین اولین کشوری بود که ژندرمانی را به نام “Gendicine” برای سر و گردن در سال 2003 تأیید کرد و پساز آن در سال 2011 روسیه “Neovasculgen” را برای بیماری عروق محیطی و در سال 2012، کمیسیون اروپا مجوز “Glybera uniQure” برای درمان تأیید کرد. تأییدیههای درمان بین سالهای 2003 تا 2012 به سرعت افزایش یافت و انتظار میرود تا سال 2025 هر سال 10 تا 20 درمان سلولی و ژنی مورد تأیید قرار گیرد. بسیاری از موفقیتهای اخیر از تاریخچه ژندرمانی را میتوان به پیشرفتهای قابلتوجه در فناوریهای ناقل ویروسی که برای تحویل مواد ژنتیکی استفاده میشود، نسبت داد.
تحولات تاریخچه ژندرمانی از سال 2010
ژندرمانی در اوایل دهه 2010، زمانیکه محققان در پنسیلوانیا و مریلند بهطور مستقل نتایج آزمایشات مربوط به درمان لوسمی یا لنفوم را گزارش کردند، شروع جدیدی داشت. درمانهای آزمایشی، سیستم ایمنی بیماران را آموزش داده و توربوشارژ میکرد تا بتوانند سلولهای سرطانی را شناسایی و از بین ببرند. برای انجام این کار دانشمندان ژنها را به گونهای مهندسی کردند تا سلولها را برای شناسایی و از بینبردن تومورها مجهز کنند. آنها این ژنها را در ناقلهای رتروویروسی به سلولهای T (سلولهای ایمنی که از خون افراد جدا شده بودند) تحویل دادند. هنگامی که سلولهای T درمانشده مجدد تزریق شدند، سرطان را به سوی بهبودی بردند.
سازمان غذا و داروی آمریکا از آن زمان تاکنون چندین مورد از درمانهای سلول T را که بهعنوان درمانهای سلول T با گیرنده آنتیژن «کایمریک» (CAR) شناخته میشوند، برای لنفومها و لوسمیها و همچنین «مولتیپل میلوما» تأیید کردهاست. در درمان “CAR T” به سلولهای T قابلیتهای شکار تومور داده میشود.
درمان الیگونوکلئوتید، یکی دیگر از رویکردهای ژنتیکی است. این تکنیک به جای اصلاح ژنهای موجود، از توالیهای کوتاهی از اسیدهای نوکلئیک یا الیگونوکلئوتیدها استفاده میکند تا بر نحوه تبدیل سلولها به پروتئینها تأثیر بگذارد؛ برای مثال در افراد مبتلا به آتروفی عضلانی نخاعی، نوسینرسن (Spinraza)، به مولکولهای RNA واسطه متصل میشود و سلولها را فریب میدهد تا پروتئین بیشتری بسازد که در افراد وجود ندارد.
عصر جدیدی از تاریخچه ژندرمانی
پیشرفت فناوری در دهه گذشته عصر جدیدی را آغاز کردهاست و تعریف ژندرمانی همچنان در حال تکامل است. جدیدترین رویکردها از تاریخچه ژندرمانی، از تحویل ژنهای سالم چشمپوشی کرده و در عوض ژنها را بهطور دقیق در داخل سلول ترمیم میکنند. این نوآوری جدید که برندهی جایزه نوبل “CRISPR-Cas9” شد، یک سیستم دفاعی ایمنی در باکتریها است که توالی DNA خاصی از ویروسهای مهاجم را شناسایی کرده و یک آنزیم را برای برش دادن و از بین بردن ژنوم ویروسی هدایت میکند. این سیستم بسیار فراتر از باکتریها کاربرد دارد و دانشمندان دریافتند که میتوانند از آن برای ایجاد برشهای دقیق در ژنوم پستانداران نیز استفاده کنند.
“Cargo” در درمانهای مبتنیبر CRISPR به وسیله ویروس، درون نانو ذره یا بهتنهایی بهعنوان کمپلکس RNA-پروتئین به سلولها وارد میشود. این روشهای درمانی را میتوان در خارج از بدن برای تغییر دادن سلولها در آزمایشگاه قبل از بازگرداندن آنها به بیمار یا با ارسال ابزارهای ویرایش ژنی مستقیما به بافتهای آسیبدیده، جایی که ژنومهای سلولی را ویرایش میکنند، استفاده کرد.
نگاهی بر تکامل و تاریخچه ژندرمانی در 10سال اخیر
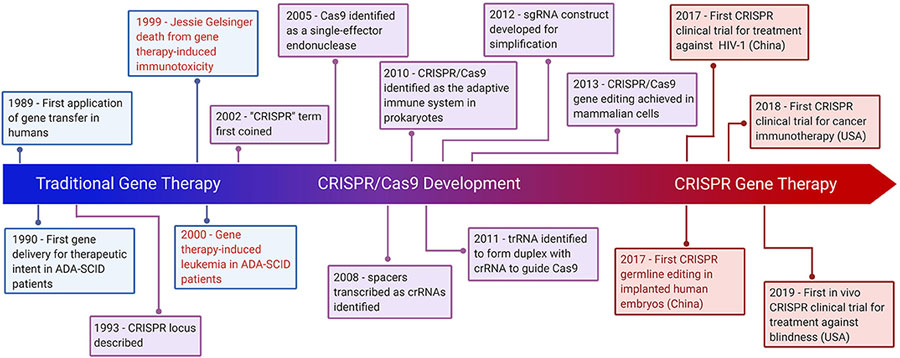
در سال 2010، اولین هستههای موثر “TAL” مهندسیشده باتوانایی ایجاد جهشزایی هدفمند توصیف شدند و همچنین برای اولینبار LLV غیرفعالکننده در آزمایشهای بالینی درمان ژن در «هموگلوبینوپاتیها» مورد استفاده قرار گرفت.
در سال 2012، آژانس دارویی اروپا “EMA” اولین درمان افزودنی ژن مبتنیبر “AAV” برای درمان کمبود لیپوپروتئین لیپاز (LPLP) را تأیید کرد و تعداد آزمایشهای بالینی تقریبا دوبرابر شد. اما این ژندرمانی در سال 2017 بهدلیل استفادهمحدود از بازار حذف شد. در این سال همچنین دانشمندان موفق به توسعهییک تکنیک ویرایش ژن بهنام CRISPR/Cas9 که میتواند توالیهای خاصی را اصلاح کند، شدند.
در سال 2016، آژانس دارویی اروپا (EMA) اولین درمان افزودنی مبتنیبر رتروویروس گاما را برای درمان نقص ایمنی ترکیبی شدید «آدنوزین دآمیناز» (ADA-SCID) تأیید کرد؛ این درمان حاوی سلولهای “CD34+” است که به ناقل رتروویروسی که توالی “cDNA ADA” را رمز گذاری میکند، تبدیل میشود.
در سال 2017، سازمان غذا و داروی آمریکا (FDA) اولین درمان افزودنی ژن در داخل بدن را برای درمان بیماران مبتلا به نوعی بیماری ارثی به نام دیستفرونی شبکیه مرتبط با جهش بی آلل “RPE65” و همچنین درمان دیگری با سلولهای CAR T را برای درمان بیماران مبتلا به لنفوم سلول B عود کننده به درمان (R/R DLBCL) تأیید کرد. همچنین “Luxturna” اولین محصول ژندرمانی ویروس مرتبط با آدنو برای آموروزیس مادرزادی نیز در سال 2017 توسط سازمان FDA تأیید شد.
در سال 2018، اولین کارآزمایی بالینی با استفاده از CRISPR/Cas9 آغاز شد. این مطالعه به بررسی استفاده از CRISPR/Cas9 برای اختلال ژن در هموگلوبینوپاتیهای بتا میپردازد.
درسال 2019، سازمان (FAD) درمان افزودنی ژنی مبتنیبر AVV را برای آتروفی عضلانی نخاعی و همچنین سازمان (EMA) درمان اضافه مبتنیبر ژن ex vivo را برای یک بیماری ژنتیکی به نام بتا تالاسمی وابسته به انتقال خون تأیید کردند. تعداد محصولات تأییدشده ژن درمانی هر سال در حال افزایش است.
درسال 2020، سازمان (FDA) دستورالعمل 6 ژندرمانی شامل پیشنویس دستورالعمل برای تحقیق و توسعه بالینی ژندرمانی را نهایی کرد.
در سال 2021، یک نوزاد چهار روزه برای آتروفی عضلانی نخاعی ژندرمانی در داخل بدن را دریافت کرد؛ این نوزاد جوانترین بیماری بود که با این ژندرمانی، مورد آزمایش قرار گرفت.
یک کارآزمایی بالینی در مراحل اولیه از روش ویرایش ژن ex vivo برای درمان افراد مبتلا به بیماری سلول داسیشکل یا مبتلا به یک اختلال خونی مرتبط به نام بتا تالاسمی استفاده کرد. این محققان نتایج را برای دو آزمایش اول خود در ژانویه 2021 گزارش کردند و در ماه ژوئن یک شرکت دیگر اولین آزمایش موفقیتآمیز ویرایش مستقیم ژن را گزارش کرد که از نانوذرات برای رساندن اجزای CRISPR-Cas9 به سلولهای کبد و غیرفعالکردن ژن دخیل در یک بیماری نادر به نام آمیلوئیدوز استفاده میکرد. اینها تنها بخشی از تاریخچه ژندرمانی در چندسال اخیر بودهاست.
چشمانداز محصولات آینده (2022-2025)
براساس آزمایشات بالینی قبلی و محصولات تأییدشده در حالحاضر، به نظر میرسد که این رشته سریعتر از همیشه در حال پیشرفت است و دهها محصول تاییدشده جدید در آینده نزدیک انتظار میرود. در حالحاضر چندین محصول در انتظار تأیید از سوی سازمانهای نظارتی هستند. با تأیید آنها، بهتدریج ژندرمانی در درمان طیف وسیعتری از بیماریها وارد میشود.
روشهای در حال ظهور امکان دقت بیشتر و مبادله نوکلئوتیدهای منفرد را فراهم کردهاند. بهعنوان مثال یا بهطور موقت فعالیت یک ژن را بدون تغییر DNA آن کاهش داده و به محققان این فرصت را میدهد تا اهداف خود را بهتر ببینند. آنها روی درمان بیماریهای عصبی، اختلالات خودایمنی و سرطانها کار میکنند. هدف آنها در درازمدت، فراتر رفتن از اختلالات تکژنی برای درمان شرایط ناشی از فعل و انفعالات چند ژن مانند؛ بیماری قلبی_عروقی و دردهای مزمن است. با درمانهای ژنتیکی که با موفقیت برخی از بیماریها را کاهش میدهد؛ محققان، پزشکان و بیماران امیدوارند که پیشرفت دهه گذشته را حفظ کنند و همچون تاریخچه ژندرمانی که نشان از پیشرفت درخشانش در این سالها دارد را بهعنوان سنگبنای پزشکی مدرن معرفی کنند.
جمعبندی
امکانات ژندرمانی بسیار نویدبخش است. مطالعه تاریخچه ژندرمانی و کارآزماییهای بالینی ژندرمانی در افراد تا حدی م را به درمان بیماریهای خاص مانند سیستم ایمنی ضعیف، هموفیلی، کوری ناشی از رتینیت پیگمانتوزا و سرطان خون امیدوار میکند. اما چندین مانع مهم بر سر راه تبدیلشدن ژندرمانی به شکل قابل اعتمادی از درمان وجود دارد مانند یافتن راهی مطمئن برای ورود مواد ژنتیکی به سلولها، هدف قراردادن سلولهای صحیح و کاهش خطر عوارض جانبی. ژندرمانی همچنان یک حوزه تحقیقاتی بسیار مهم و فعال با هدف توسعه درمانهای جدید و مؤثر برای انواع بیماریها است.
نویسندگان: یاسمن اسمی، کوثر حاجیپور
منابع
تهیـهشـده در آکـــادمـی ژنـــتیـــک ایــران
همچنین بخوانید: تاریخچه ژندرمانی در سالهای 2010_1996