فهرست مطالب
اپیژنتیک در بیماریهای خودایمن بهطور مستقیم و غیرمستقیم اثرگذار است. بهطور کلی، اپیژنتیک مطالعه چگونگی بیان ژن سلولها بدون تغییر توالی DNA است.
در رابطه با بیماریهای خودایمن و اپیژنتیک در ابتدا شناخت اپیژنتیک حائز اهمیت است. اپی در لغت بهمعنای بالا یا بالاتر است و اپیژنتیک، عواملی بیشتر از کد ژنتیکی را توصیف میکند. تغییرات اپیژنتیکی تغیراتی هستند که بیان یا عدمبیان ژنها را تنظیم میکنند. در مجموعه کامل DNA در یک سلول، تمام تغییراتی که بیان ژنها را تنظیم میکنند، بهعنوان اپیژنوم شناخته میشوند. اپیژنوم شامل افزودن گروههای شیمیایی در DNA و پروتئینهای هیستونی یک موجود است. این تغییرات را میتوان از طریق توارث اپیژنتیکی به زادههای ارگانیسم منتقل کرد. تغییراتی که در اپیژنوم اتفاق میافتد، باعث تغییر در ساختمان کروماتین و تغییر در عملکرد ژنوم شود.
روشهای اثرگذاری اپی ژنتیک در بیماری های خود ایمن
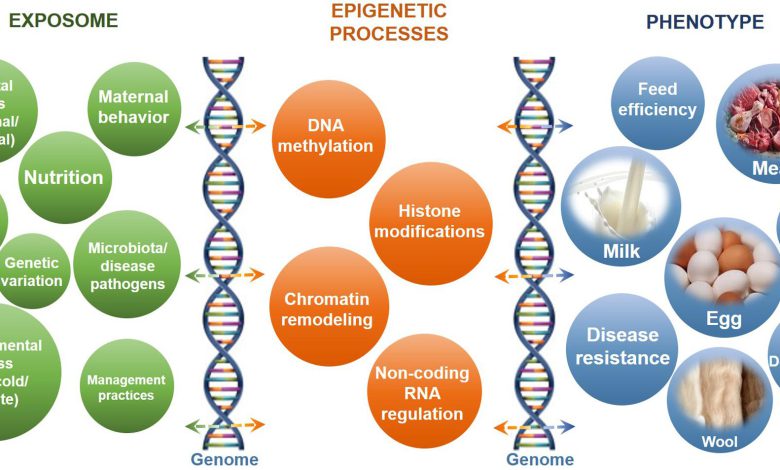
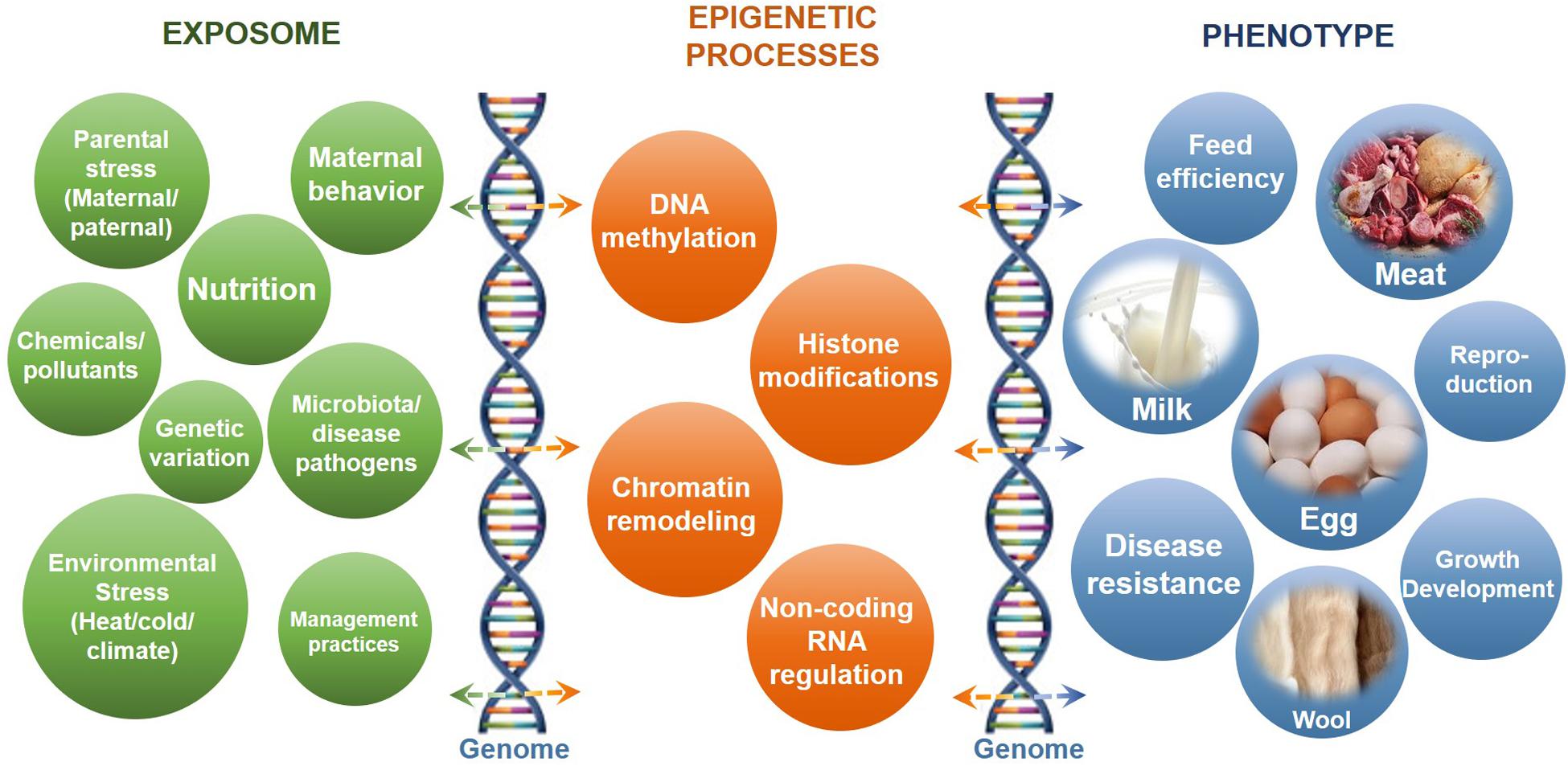
ما به دنبال کشف ردپای اپیژنتیک در بیماریهای خود ایمن هستیم. اپی ژنتیک به روشهای مختلف بر بیان ژنهای تاثیرگذار در بیماریهای خودایمن اثر میگذارد. انواع تغییرات اپیژنتیکی عبارتاند از:
- فرآیند متیلهکردنDNA: متیلاسیون DNA با اضافهکردن یک گروه شیمیایی به DNA عمل میکند. بهطور کلی، این گروه به مکانهای خاصی روی DNA اضافه میشود و پروتئینهای متصل به DNA را برای بیان ژن مسدود میکند. این گروه شیمیایی را میتوان از طریق فرآیندی به نام دیمتیلاسیون حذف کرد. بهطور معمول، متیلاسیون باعث بیان ژنها و دمتیلاسیون باعث عدم بیان ژنها میشود.
- تغییرات پروتئینهای هیستونی:گروههای شیمیایی را میتوان به هیستونها برای بستهبندی DNA اضافه یا حذف کرد. DNA برای فشردهسازی بهتر به دور پروتئینهای هیستونی میچرخد، هنگامی که DNA محکم به دور هیستونها پیچیده باشد، پروتئینهایی که بیان ژن را انجام میدهند نمیتوانند بهراحتی به DNA دسترسی پیدا کنند، بنابراین بیان ژن خاموش میشود. وقتی DNA به دور هیستونها به شکل درستی پیچیده نشدهباشد، مقدار DNA در دسترس پروتینهای بیان ژن بیشتر میشود، بنابراین بیان ژن روشن میشود.
- RNAهای غیرکدکننده: DNA بهعنوان مرکزی از دستورالعملها برای ساختن RNA کدکننده و غیرکدکننده استفاده میشود. RNA کدکننده برای تولید پروتئین استفاده میشود. RNA غیرکدکننده با اتصال به RNA کدکننده همراه با یک سری از پروتئینهای خاص، در کنترل بیان ژن نقش ایفا میکند تا RNA کدکننده را تجزیه کند، تا نتوان از آن برای تولید پروتئین استفادهکرد. RNA غیرکدکننده ممکن است پروتئینها را برای تصحیح هیستونها در رابطه با روشن یا خاموششدن ژنها به کار گیرد.
- میکروRNAها: MicroRNAها مولکولهای RNA غیرکدکننده کوچک و بسیار حفاظتشدهای هستند که در تنظیم بیان ژن نقش دارند. MicroRNAها توسط RNA پلیمرازهای II و III رونویسی میشوند و پیشسازهایی تولید میکنند که تحت یک سری رویدادهای خاص، microRNAهای بالغ را تشکیل میدهند.
روشهای سیر تکاملی اپیژنتیک
- اپیژنتیک و نمو: تغییرات اپیژنتیک قبل از متولدشدن شروع میشود، همه سلولها دارای ژنهای یکسان هستند، اما ظاهر و عملکرد متفاوتی دارند. طی پروسهی رشد، اپیژنتیک به تعیین عملکرد یک سلول کمک میکند، بهعنوان مثال: تبدیل سلولها به سلول قلبی، سلول عصبی و سلول پوستی.
- اپیژنتیک و سن: اپیژنتیک در مراحل مختلف زندگی تغییر میکند. اپیژنتیک در بدو تولد با اپیژنتیک در دوران کودکی یا بزرگسالی یکسان نیست.
- اپیژنتیک و برگشتپذیری: همه تغییرات اپیژنتیک دائمی نیستند؛ برخی تغییرات اپیژنتیکی را میتوان در پاسخ به تغییرات رفتار یا محیط اضافه یا حذف کرد.
آنچه باید در رابطه با بیماریهای خودایمنی بدانید…

در این مطلب، ما به دنبال کشف و بررسی تاثیر و رابطهی اپیژنتیک در بیماریهای خودایمن هستیم. بیماریهای خود ایمنی زمانی رخ میدهند که سیستم ایمنی بدن به اشتباه به سلولهای بافت سالم بدن حمله میکند و آنها را از بین میبرد؛ در بدن انسان، میتواند بیش از 80 اختلال خودایمنی وجود داشته باشد. سلولهای خونی در سیستم ایمنی بدن به محافظت در برابر مواد مضر کمک میکنند.
بهعنوان مثال میتوان به باکتریها، ویروسها، سموم، سلولهای سرطانی، خون و بافت خارج از بدن اشاره کرد. این مواد حاوی آنتیژن هستند. سیستم ایمنی علیه این آنتیژنها، آنتیبادیهایی تولید میکند که آن را قادر میسازد این مواد مضر را از بین ببرد. هنگامی که شما یک اختلال خودایمنی دارید، سیستم ایمنی بدن شما بین بافت سالم و آنتیژنهای مضر بالقوه، تمایز قائل نمیشود. در نتیجه، بدن شما واکنشی را انجام میدهد که بافتهای طبیعی را از بین میبرد.
علت دقیق اختلالات خودایمنی ناشناخته است؛ براساس نظریهای، برخی از میکروارگانیسمها (مانند باکتریها یا ویروسها) یا داروها ممکن است باعث ایجاد تغییراتی شوند که سیستم ایمنی را دچار اشتباه کند. این موضوع بیشتر در افرادی اتفاق میافتد که دارای ژنهایی هستند که آنها را مستعد ابتلا به اختلالات خودایمنی میکند. تخریب یا ازهمگسیختگی بافتهای بدن توسط سیستمایمنی، بهدلیل تعامل پیچیده عواملژنتیکی و محیطی است. جمعیتی مانند موشها و انسان حاوی مجموعهای از جهشهای DNA یا انواع آللی هستند که بر بیان عملکرد ژنهای دخیل در کنترل پاسخ ایمنی تاثیر میگذارند.
اسکن کل ژنوم برای پلیمورفیسمهای رایج مرتبط با بیماری، منجر به شناسایی ژنهای خطرناک جدید متعددی شدهاست که در فنوتیپهای خودایمنی دخیل هستند. اختلالات خودایمنی اساس ژنتیکی پیچیدهای دارند و ژنهای متعددی در خطر ابتلا به بیماری نقش دارند که هر کدام بهطور مستقل، دارای اثرات متوسط هستند. بیماریهای خودایمنی میتوانند در اثر موارد زیر ایجاد شوند:
- تخریب بافت بدن؛
- رشد غیرطبیعی یک اندام؛
- تغییر عملکرد یک اندام.
اختلالات خودایمنی ممکن است یک یا چند نوع اندام یا بافت را تحتتاثیر قرار دهد. مناطقی که اغلب تحتتاثیر اختلالات خودایمنی قرار میگیرند عبارتاند از:
- رگهای خونی؛
- بافت همبند؛
- غدد درونریز مانند: تیروئید و پانکراس؛
- مفاصل؛
- ماهیچهها؛
- سلولهای قرمز خون؛
- پوست.
ردپای اپیژنتیک در بیماریهای خودایمن
تغییرات اپیژنتیکی در بیماریهای خودایمن بر بیان ژن تاثیر میگذارد و عملکرد سلولی را بدون تغییر توالی ژنومی تغییر میدهد. متیلاسیون دینوکلئوتیدهای DNA CpG و یا هیدروکسی متیلاسیون آنها، تغییرات پس از ترجمه انتهای اسیدآمینه پروتئینهای هیستون و بیان RNA غیرکدکننده، رویدادهای اپیژنتیکی اصلی هستند. مکانیسمهای اپیژنتیک، پنجرهای برای درک مکانیسمهای احتمالی درگیر در پاتوژنز بیماریهای پیچیده مانند بیماریهای خودایمنی هستند. قابل توجه است که بیماریهای خودایمنی اپیدمیولوژی، آسیبشناسی یا علائم یکسانی ندارند، اما منشا مشترکی دارند که میتواند با اشتراک مکانیسمهای ایمنی ژنتیکی توضیح دادهشود.
رویدادهای اپیژنتیکی بهعنوان عوامل پاتوفیزیولوژیک مرکزی علاوهبر استعداد بیماری ژنتیکی و بهعنوان عوامل کمکی تعیینکننده، تصاویر بالینی و نتایج در افراد مبتلا به بیماری تک ژنی شناسایی شدهاست. بنابراین، درک کامل عوامل اپیژنتیک در بیماری خودایمنی منجر به رویکردهایی برای پیشبینی پیامدهای بیماریفردی و معرفی درمانهای مؤثر، هدفمند و قابل تحمل میشود. یافتههای اخیر را که نشاندهنده اپیژنتیک و نقش آن در بیماریهای خودایمن است، با انتخاب سه مثال خلاصه میکنیم:
- بیماری خود التهابی استخوان استئومیلیت مزمن غیرباکتریایی (CNO)؛
- اختلال (الگوی مختلط) پسوریازیس؛
- بیماری خودایمنی سیستمیک لوپوس اریتماتوز (SLE).
بیماری خودالتهابی عفونت استخوان مزمن غیرباکتریایی (CNO)
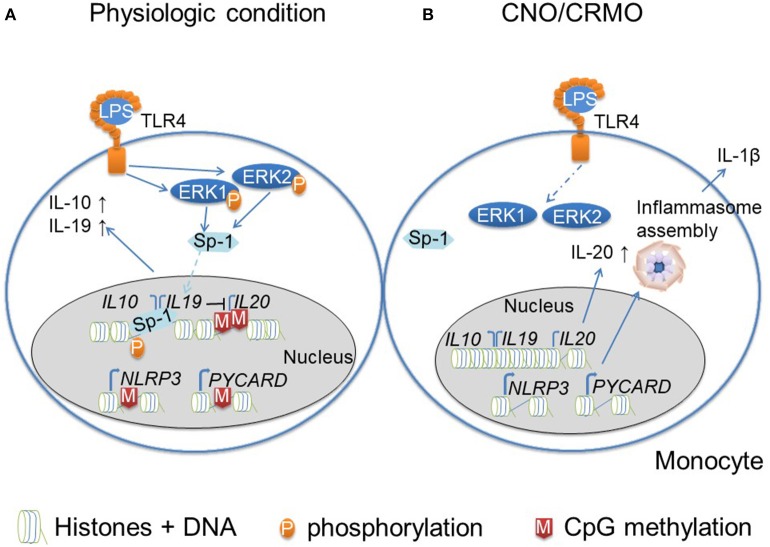
در پاسخ به فعالسازی TLR4 (به همراه لیپوپلیساکارید؛ LPS) مونوسیتهای افراد سالم، پروتئین کینازهای فعالشده با میتوژن (MAPK)، کینازهای واکنشی سیگنال خارج سلولی (ERK)1 و 2 را فسفریله میکنند. کینازها فاکتور تنظیمکننده رونویسی را فعال میکنند و منجر به انتقال آن به هسته میشوند. علاوهبر این، ERK1/2 به فسفوریلاسیون هیستون H3 در باقیمانده سرین 10 (H3S10) کمک میکند که منجر به ساختار کروماتین باز در IL10 و IL19 میشود.
این رویدادها با هم، منجر به ترانس فعالشدن IL10 و IL19 میشود. بیان سیتوکین تنظیمکننده ایمنی (IL-10 و IL-19) بر بیان IL-20 عضو خانواده سیتوکینهای پیش التهابی IL10 تاثیر منفی میگذارد. علاوهبر این، پروموتر IL20 توسط متیلاسیون DNA CpG کنترل میشود.
Inflammasomeها مجتمعهای چند پروتئینی هستند که در پاسخ به سیگنالهای خطر، فعال میشوند. علاوهبر این، بیان اجزای التهابی (NLRP3 و ASC/PYCARD) توسط رویدادهای اپیژنتیکی تنظیم میشود. پروموتورهای NLRP3 و PYCARD توسط متیلاسیون DNA CpG کنترل میشوند. (B) در مونوسیتهای بیماران CNO/CRMO، فعالسازی ERK1/2 در پاسخ به تحریک LPS مختل میشود که منجر به کاهش فعالسازی Sp-1 و جابهجایی هستهای و کاهش فسفوریلاسیون H3S10 در IL10 و IL19 میشود که منجر به اختلال در بیان ژن میشود.
کاهش سطح بیان سیتوکین تنظیمکننده ایمنی، بیان بالاتری از سیتوکین پیشالتهابی IL-20 را فراهم میکند. علاوهبر این، اختلال در بیان IL-10 و IL-19 بیان اجزای التهابی را افزایش میدهد و متیلاسیون DNA CpG ژنهای PYCARD و NLRP3 را کاهش میدهد و بیان مولکولهای پیش التهابی را افزایش داد. بنابراین، رویدادهای اپیژنتیک در پاتوفیزیولوژی مولکولی CNO/CRMO نقش دارند.
اختلال «الگوی مختلط» پسوریازیس
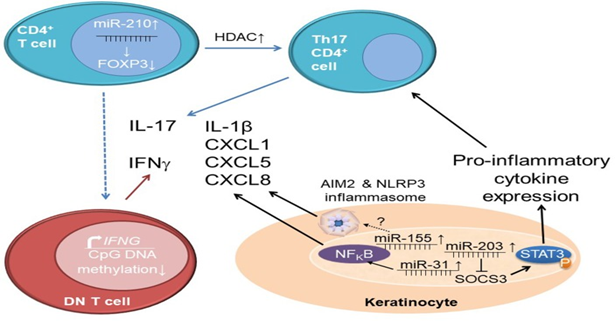
اپیژنتیک هماهنگکننده تعاملات بین سلولهای ایمنی و استروما در پسوریازیس است، افزایش بیان miR-210 در سلولهای CD4+ T از بیماران پسوریازیس، بیان مولکول تنظیمکننده ایمنی FOXP3 را کاهش میدهد. همراه با افزایش سطح هیستون داستیلاز (HDAC) که به افزایش بیان سیتوکینهای پیشالتهابی (به ویژه IL-17A) کمک میکند، منجر به عدم تعادل بین سلولهای T موثر (سلول Th17) و سلولهای T تنظیمی میشود. سلولهای T دوگانه منفی (DN) CD3 + CD4-CD8- در بیماران پسوریازیس، بهطور اپیژنتیکی برای بیان IFN-γ از طریق کاهش متیلاسیون DNA CpG در یک عنصر تقویتکننده دیستال ژن IFNG آماده شدهاند.
کراتینوسیتهای بیماران پسوریازیس بیان miR-203 را افزایش میدهند که منجر به کاهش بیان SOCS3، تنظیمکننده منفی سیگنالدهی STAT3 میشود. این به افزایش فسفوریلاسیون (فعالسازی) STAT3 کمک میکند و متعاقبا بیان سیتوکینهای پیش التهابی و تمایز سلولهای T موثر را افزایش میدهد. بیان miR-31 در کراتینوسیتها به فعالشدن NFκB و تولید متعاقب آن IL-1β، CXCL1،-5 و-8 کمک میکند. سطوح بالا از miR-155 باعث تحریک AIM2 و NLRP3 التهابی از طریق مکانیسمهای ناشناخته میشود که منجر به افزایش انتشار IL-1β میشود.
بیماری خودایمنی سیستمیک لوپوس اریتماتوز (SLE)
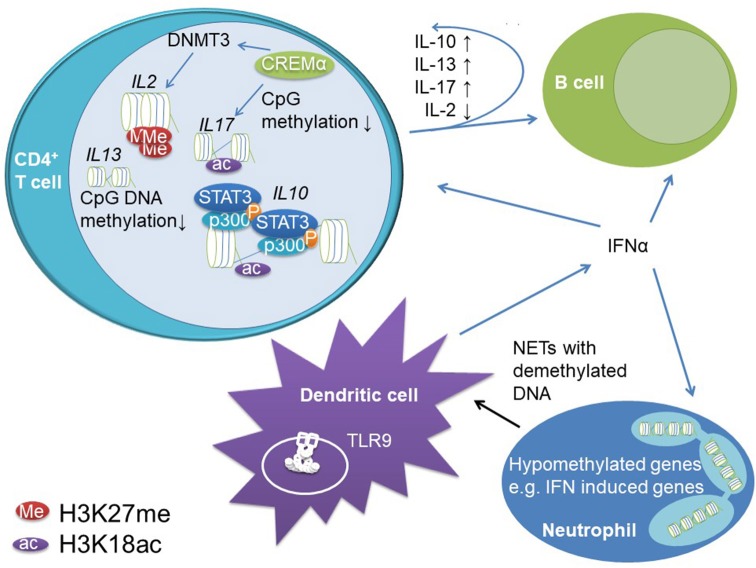
مکانیسمهای اپیژنتیک، به اختلال در تنظیم پاسخهای ایمنیذاتی و سازگار در SLE کمک میکند. کاهش متیلاسیون DNA CpG در نواحی تنظیمی IL10 و IL13 باعث افزایش بیان ژن میشود. STAT3 به عناصر تنظیمکننده IL10 در پروموتر پروگزیمال و یک تقویتکننده ذاتی جذب میشود.
در این عناصر، STAT3 فعالکننده رونویسی p300 را که دارای فعالیت هیستوناستیلاز است و از تجزیه کروماتین از طریق H3K18ac و افزایش بیان ژن پشتیبانی میکند، به کار میگیرد. افزایش بیان IL-10 در سلولهای T باعث افزایش فعالیت سلولهای B در SLE میشود؛ این درحالی است که بر سلولهای T موثر تاثیر نمیگذارد (احتمالاا به دلیل کاهش بیان گیرنده IL-10 در سلول های T از بیماران SLE).
واسطه عنصر، پاسخ cAMP فاکتور رونویسی (CREM)α سلولهای T موثر را در SLE ارتقا میدهد. این استیلاسیون H3K18 و دمتیلاسیون DNA CpG را در سراسر خوشه ژن IL17 القا میکند؛ درحالیکه DNMT3 را به منبع IL2 که متیلاسیون DNA را آموزش میدهد، جذب میکند. علاوهبر این، CREMα هیستون داستیلاز (HDAC)1 را به ژن IL2 جذب میکند که منجر به کاهش H3K18ac و خاموششدن ژن پایدار میشود.
علاوهبر این، سلولهای B و T با افزایش بیان IFN نوع I (IFN-α و -β) در سلولهای دندریتیک و نوتروفیلها تحریک میشوند. نوتروفیلها، کاهش متیلاسیون DNA CpG را در IFNهای نوع I و ژنهای مرتبط نشان میدهند. سلولهای دندریتیک برای آزادسازی IFN نوع I از طریق تحریک TLR9 اندوزومی از طریق NETosis افزایشیافته نوتروفیلها آماده میشوند. نوتروفیلهای بیماران SLE DNA هیپومتیله را آزاد میکنند که در مقایسه با DNA متیله، قویتر به TLR9 متصل میشود.
سخن پایانی
اپیژنتیک از بدو تولد و در طول زندگی انسان مرتبا تغییر میکند، این تغییر به گونهای نیست که روی توالی DNA تغییری ایجاد کنند و آسیبی به ژنوم سلولها وارد کند. در بحث نقش اپیژنتیک در بیماریهای خودایمن، با نقض قضیهی عدم آسیبرسانی و ایجاد جهش رو به رو میشودیم. به گونهای که در این بین اپیژنتیک باعث ایجاد بیماریهای مختلفی میگردد که بیماریهای خودایمن تنها گوشهای از این نوع بیماریهای تاثیریافته از نقش اپیژنتیک است.
نویسنده: هما پورافشار
منابع:
1.https://medlineplus.gov/genetics/understanding/howgeneswork/epigenome
2.https://www.cell.com/fulltext/S0092-8674(00)81110-1
3.https://www.cdc.gov/genomics/disease/epigenetics.htm#:~:text=Epigenetics%20is%20the%20study%20of,body%20reads%20a%20DNA%20sequence
4.https://pubmed.ncbi.nlm.nih.gov/31333659
