فهرست مطالب
درمان سرطان و نانوپزشکی
تحقیقات وسیع موسسهی MIT با کشف مناسبترین نانوذرات برای هدف قراردادن انواع سلولهای خاص، از سلول سرطانی گرفته تا سلولهای ایمنی و انواع دیگر سلولهای عضو سالم و بیمار، به واسطه نشانگرهای زیستی، میتواند موجب پیشرفت نانوپزشکی در درمان سرطان شود.
محققان موسسهی MIT یک روش غربالگری با کارایی بسیار بالا انجام دادند که به آنها اجازه داد بهطور سیستماتیک برهمکنش ۳۵ نوع نانوذرهی مختلف را با ۵۰۰ ردهیسلول سرطانی ارزیابی کنند. صفحه نمایشهای نانوذرات برای بهینهسازی خواص مواد در زمینههای بیولوژیکی خاصی طراحی شدهاند. با استفاده از این رویکرد، محققان MIT اطلاعات بسیار زیادی درمورد ویژگیهای سلولهای سرطانی و نانوذرات را شناسایی کردند که میتوانند وارد کردن مواد درمانی به سلولهای سرطانی از طریق جذب نانوذرات را پیشبینی کنند این باعث پیشرفت بیشتر در درمان سرطان و توسعهی داروهای مبتنی بر نانوذرات میشود.
یافتههای این مطالعه به محققان نانوپزشکی کمک میکنند تا با کشف نقش خواص شیمیایی و سایر خواص نانوذرات در هدفگیری سلولهای سرطانی، ذرات دارویی خود را با انواع خاصی از سرطان تطبیق دهند یا نانوذرات جدیدی طراحی کنند که از ویژگیهای بیولوژیکی انواع خاصی از سلولهای سرطانی بهره میبرند.
تحول درمان سرطان با نانوذرات نجاتبخش
نانوذرات بهطور فزایندهای به عنوان وسیلهای دقیق برای دارورسانی بهمنظور درمان سرطان مورد آزمایش قرار میگیرند و برخی از آنها در حال حاضر برای شیمیدرمانی سرطان مورد استفاده بالینی در نانوپزشکی قرار دارند. درمانهای مبتنی بر نانوذرات میتوانند مزایای درمانی مختلفی مانند کاهش سمیت، نیمهعمر طولانیتر و بهبود دارورسانی ارائه دهند. اگرچه، تعداد زیادی از فرمولهای نانوذراتی با خواص فیزیکی و بیولوژیکی متفاوت وجود دارند، اما مشخص نیست که کدام یک از آنها در شرایط وقوع یک بیماری خاص بهترین عملکرد را دارند.
استفاده از عوامل درمانی با واسطهی نانوذرات این پتانسیل را دارند که بهطور قابلتوجهی بر روند درمان سرطان بهویژه در زمینهی درمان سرطان شخصیسازیشده، تأثیر بگذارند. نانوذرات طیف متنوعی از مواد و خواص را در بر میگیرند. آنها را میتوان برای محصورکردن و محافظت از طیف گستردهای از محمولههای درمانی، از جمله مولکولهای کوچک بیولوژیک و اسیدهای نوکلئیک طراحی کرد.
موانع استفاده از نانوذرات درمانی
یک چالش مهم در استفاده موفق نانوذرات، درک ناقص از تعاملات نانوزیستی در محل اعمال بیومولکولهای موردنظر است. محققان قبلاً انواع مختلفی از نانوذرات را تولید کرده بودند که توان رساندن دارو به سلولهای سرطانی را داشتند، اما انواع مختلف سلولهای سرطانی اغلب به نانوذرات یکسان پاسخ متفاوتی میدادند. تاکنون تنها تعداد انگشتشماری از داروهای سرطان مبتنی بر نانوذرات مورد تایید FDA قرار گرفتهاند.
زیستشناسان براي کشف تفاوتهای بیولوژیکی بین سلولها که میتواند باعث تغییر در پاسخهای آنها به نانوذرات و بهبود روند درمان سرطان شوند، تصمیم گرفتند در یک پروژهی تحقیقاتی گسترده انواع سلولهای سرطانی مختلف که با بسیاری از انواع نانوذرات در تعامل هستند را بررسی کنند.
بررسی تعاملات سلول و نانوذره با پلتفرم PRISM
پلتفرم PRISM یک برنامهی گرافیکی علمی است که در زمینهی آنالیز داده، دستهبندی نمودارها، به اشتراکگذاشتن دادهها و منحنیها در نانوپزشکی کاربرد دارد. نرم افزار PRISM که توسط موسسه Broad ساخته شده، محققان را قادر میسازد تا به سرعت هزاران دارو را روی صدها نوع مختلف سلولهای سرطانی بهطور همزمان غربالگری کنند. این تیم به جای آزمایش روی تعاملات سلولی دارویی از پلتفرم PRISM برای غربالگری فعل و انفعالات سلول- نانوذرات استفاده کردند. دانشمندان بخش سرطان MIT با استفاده از این رویکرد توانستند به این سوال پاسخ دهند که آیا ژنوتیپ سلولهای سرطانی میتواند بر روی میزان جذب نانوذره در درمان سرطان موثر باشد یا خیر.
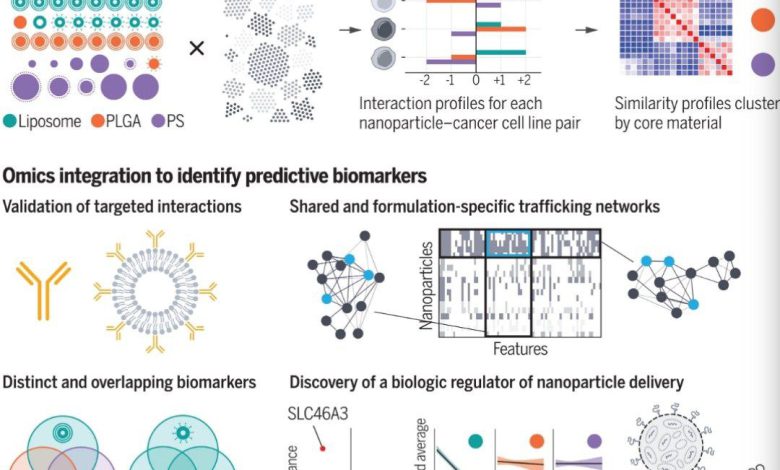
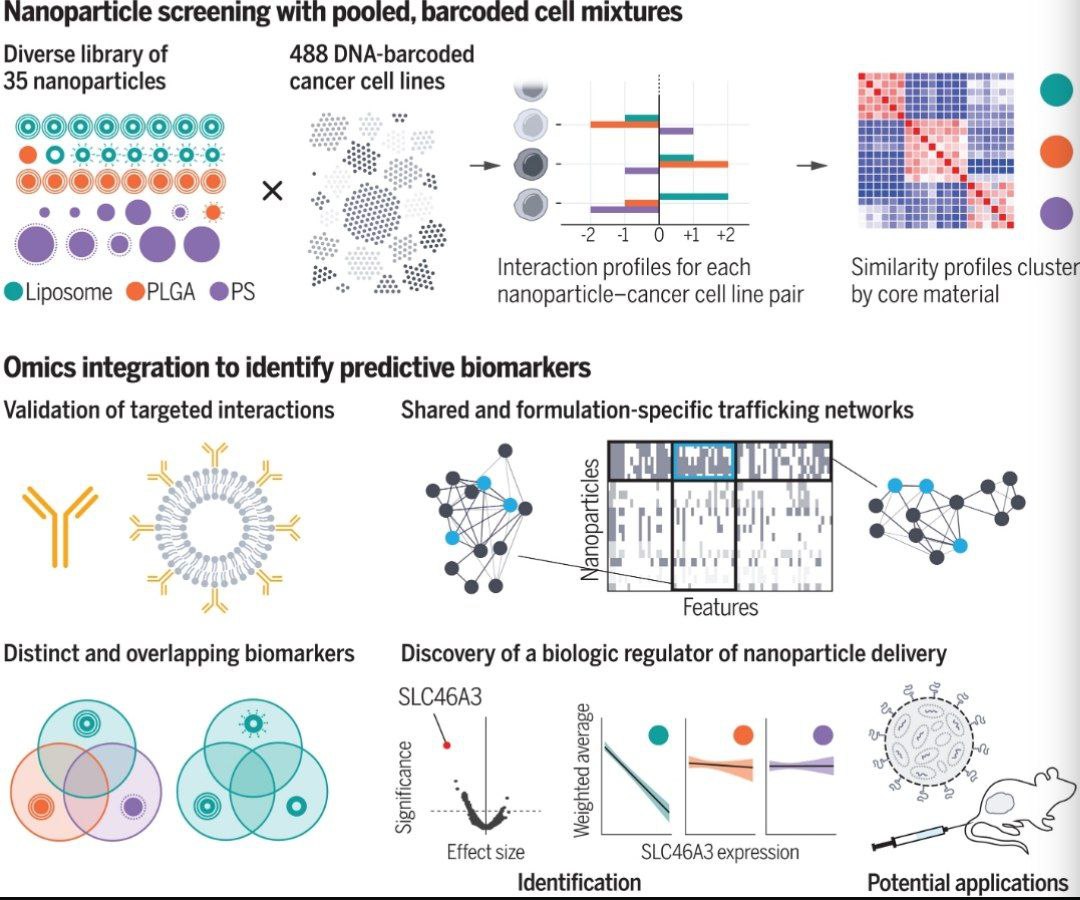
کپشن عکس: صفحه نمایش nanoPRISM فرآیند دارورسانی نانوذرات و omics و را ادغام میکند. با استفاده از یک کتابخانه نانوذرات انتخاب شده، پروفایلهای تعامل نانوذرات و سلولها، صدها سلول سرطانی را بهطور همزمان غربال شد. با ترکیب حاشیهنویسی omics، ویژگیهای بیولوژیکی یا نشانگرهای زیستی را شناسایی شد که واسطهی انتقال نانوذرات به سلولها هستند و یک تنظیمکننده بیولوژیکی برای دارورسانی نانوذرات مبتنی بر لیپید کشف شد. PLGA، پلیلاکتید-کو-گلیکولید؛ PS، پلی استایرن.
آزمایشی گسترده با نمونههای زیاد و متنوع سلولهای سرطانی
محققان MITبراي صفحه نمایش PRISM از ۴۸۸ ردهیسلولهای سرطانی از ۲۲ بافت مختلف استفاده کردند. برای هر نوع سلول با یک توالی DNA منحصر به فرد، بارکدی را تعیین کردند تا در مراحل بعد قابل شناسایی باشند. برای هر نوع از سلولهای سرطانی مجموعه دادههای گستردهای در مورد بیان ژن و سایر ویژگیهای بیولوژیکی موثر در درمان سرطان به دست آمد.
محققان ۳۵ نانوذره ایجاد کردند که هر یک دارای هستهای متشکل از لیپوزوم (ذراتی که از مولکولهای چربی به نام لیپیدها ساخته شدهاند) بودند، که پلیمری به نام PLGA یا پلیمر دیگری به نام پلیاستایرن در خود دارا بودند؛ همچنین نانوذرات را با انواع مختلفی از مولکولهای محافظ یا هدف از جمله پلیمرهایی مانند پلیاتیلنگلیکول، آنتیبادیها و پلیساکاریدها ترکیب کردند. این کار به آنها اجازه داد تا تأثیر ترکیب هسته و سطح شیمیایی نانوذرات را مطالعه کنند.
نانوذرات اختصاصی به سمت سلولها میروند
محققان MIT، استخرهایی از صدها سلول مختلف را در معرض هر یک از ۳۵ نانوذره مختلف قرار دادند. هر کدام از نانوذرات دارای برچسب فلوئورسنت بودند؛ بنابراین امکان جداسازی سلولها براساس میزان فلورسانس آنها پس از قرار گرفتن ۴ الی ۲۴ ساعت در معرض نانوذرات وجود داشت. براساس این اندازهگیریها، به هر ردهیسلولی امتیازی اختصاص داده شد که نشاندهندهی میل ترکیبی آن برای هر نانوذره است. سپس محققان از الگوریتمهای ماشین لرنینگ برای تجزیه و تحلیل این امتیازات به همراه سایر دادههای بیولوژیکی موجود برای هر ردهی از سلولهای سرطانی استفاده کردند.
نشانگرهای زیستی تعیینکنندهی تمایل سلول سرطانی به دریافت محموله نانوذره
این تجزیه و تحلیل نتایج بسیار گستردهای مربوط به ویژگیهای سلولهای سرطانی یا نشانگرهای زیستی مرتبط با میل ترکیبی برای انواع مختلف نانوذرات را به همراه داشت. بسیاری از این نشانگرهای زیستی، ژنهایی بودند که ماشینهای سلولی مورد نیاز برای اتصال ذرات، واردکردن آنها به سلول یا پردازش آنها را کد میکردند. برخی از این ژنها قبلاً در ورود نانوذرات نقش داشتند اما بسیاری دیگر جدید بودند. یافتههای این تحقیق کمک بزرگی به توسعهی دیدگاه محققان نانوپزشکی در مورد نحوهی تعامل نانوذرات و سلولهای سرطانی در روند درمان سرطان میکنند.
جذب نانوذرات و نقش مهم پروتئین SLC46A3
محققان MIT یکی از نشانگرهای زیستی (پروتئین SLC46A3) را بیشتر مورد بررسی قرار دادند. صفحه نمایش PRISM نشان داده که سطوح بالای این پروتئین با جذب بسیار کم نانوذرات مبتنی بر لیپید، همبستگی دارد. آزمایش این نانوذرات در مدل موش ملانوما همبستگی مشابهی را نشان داد. این نشانگرهای زیستی میتوانند برای کمک به پزشکان در شناسایی بیمارانی که تومورهایشان بیشتر به درمانهای مبتنی بر نانوذرات پاسخ میدهند، استفاده شوند.
محققان MIT در تلاشاند مکانیسم تنظیم جذب نانوذرات توسط SLC46A3 را در تومورها کشف کنند. درصورتیکه راههای جدیدی برای کاهش سطوح سلولی این پروتئین کشف شود، میتوانند موجب حساسیت بیشتر تومورها در برابر نانوذرات لیپیدی در درمان سرطان شده و روشهای درمانی نانوپزشکی را ارتقا دهد.
ردپای فاکتور رشد اپیدرمی در کاهش اثر نانوذرات بر سلول
برای بررسی ویژگیهای سلولهای سرطانی که بر ارتباط نانوذرات حاکم هستند، از تحلیلهای همبستگی دادهها استفاده شد. بهطور معنیدار بیان بالای ژن گیرنده فاکتور رشد اپیدرمی (EGFR) و فراوانی پروتئین آن را به عنوان نشانگرهای زیستی که تمایل سلولی را برای الگوهای ضد EGFR پیشبینی میکنند، شناسایی شد. به طور کلی، مواد هستهی نانوذره و همچنین اصلاح سطح سلول بر تعداد و اهمیت بیومارکرهایی که جذب نانوذرات را در تومور پیشبینی میکنند، تأثیر میگذارد.
نتایج
دانشمندان موسسهی MIT با طراحی کتابخانهی نانوذرات فلورسنت، اثرات طیف وسیعی از پارامترهای نانوذرات از جمله ترکیب هسته، شیمی سطح و اندازه بر تعاملات سلولهای سرطانی ثبت کردند و برهمکنشهای هر نانوذره را با رده سلولی سرطانی بارکد شده را غربالگری و قدرت ارتباط سلولها با نانوذرات را شناسایی کردند. صفحه نمایشی برای کاوش در دارورسانی نانوذرات طراحی شد و نشان داد به طور کلی، مواد هستهی نانوذره و همچنین اصلاح سطح آن بر تعداد و اهمیت بیومارکرهایی که جذب را ممکن میکنند، تأثیر میگذارد. بسیاری از نشانگرهای زیستی با ژنهای مسئول جذب مواد، انتقال و چسبندگی مرتبط بودند. الگوریتمهای ماشین لرنینگ، نشانگرهای زیستی پیشبینیکنندهی شبکههای تعامل پروتئین-پروتئین را شناسایی کرد.
در مطالعهی موسسهی MIT، نشانگرهای زیستی خاصی فرمول نانوذرهای را به دست آورد که بیان ژن SLC46A3 ، به عنوان یکی از نشانگرهای زیستی پیشبینیکننده برای جذب نانوذرات مبتنی بر لیپید در تومور را اثبات و همچنین کارایی انتقال محمولههای اسیدنوکلئیک را را تأیید کرد.
چشمانداز آینده
این رویکرد غربالگری همچنین میتواند به محققان برای بررسی بسیاری از انواع دیگر نانوذرات حامل برای درمان تومور کمک کند. در عصر پزشکی تخصصی که تمرکز اصلی بر روی ارائه درمانهای هدفمند مولکولی به بخشهای درون سلولی خاص وجود دارد، بررسی رابطهی ساختار-عملکرد نانوذرات به دلیل ارتباط آنها با ناهمگنی سلولی و بیولوژیکی نقش مهمی در نانوپزشکی دارد. ترکیب غربالگری تلفیقی با حاشیهنویسی چندوجهی، پتانسیل تسریع هدفیابی سلولهای سرطانی و تنظیمکنندههای ناشناخته را دارد و میتواند نشانگرهای زیستی نانوذرات وارد شده به سلولهای تومور را در کمترین زمان ممکن شناسایی کند.
نویسنده:مطهره نوعی
ویراستار:سارا تاجداری
منابع

یک نظر