فهرست مطالب
آزمایش آنتیبادی ریبونوکلئوپروتئین ضدهستهای
آنتیبادیهای آنتیژن RNP (که در ابتدا anti-Mo نامیده میشد) با استفاده از ID در سرمهای بیماران مبتلا به systemic lupus erythematosus یا به اختصار SLE توسط Mattioli و Reichlin در سال 1971 شناسایی شدند. اصطلاح RNP از مشاهدات اولیهای ناشی میشود، که فعالیت آنتیژنی آن میتواند با درمان با ریبونوکلئاز و تریپسین از بین برود. بنابراین این یک آنتیژن ریبونوکلئوپروتئین یا «پروتئین RNA » بیان میشود، در حالیکه آنتیژن Sm در برابر چنین درمانی مقاوم است.
در سال 1971، شارپ و همکاران گروهی از بیماران مبتلا به سندرمی را توصیف کردند که با ویژگیهایSLE ، بیماری التهابی عضلانی و اسکلرودرمی، با عدم وجود بیماری کلیوی مشخص میشود و آن را بیماری بافت همبند مختلط (MCTD) نامیدند. سرم این بیماران حاوی آنتیبادیهایی برای ENA بود که با هماگلوتیناسیون غیرفعال اندازهگیری شد. مطالعات بعدی نشان داد که ENA حاوی هر دو آنتیژن Sm و RNP (10-18) است و بیمارانی که توسط شارپ و همکاران توصیف شدهاند با RNP واکنش نشان میدهند. در سال 1979، لرنر و استیتز نشان دادند که هر دو آنتیژن Sm و RNP روی U1 snRNP قرار دارند. بنابراین آنتی RNP گاهیاوقات بهعنوان آنتیبادیهای anti-U1 RNP و anti-U1 snRNP نیز شناخته میشود.

RNP (همچنین nRNP و U1RNP نامیده میشود( یک ریبونوکلئوپروتئین هستهای کوچک است که حاوی 3 اتوآنتیژن پروتئینی) به نامهای A ، C و (kD68 است. سرمهایی که حاوی آنتیبادیهای RNP هستند عمدتاً با اتوآنتیژنهای A و kD-68 واکنش نشان میدهند. آنتیبادیهای RNP تقریباً در 50٪ از بیماران مبتلا به لوپوس اریتماتوز (LE) و در بیماران مبتلا به سایر بیماریهای بافت همبند، به ویژه بیماری بافت همبند مختلط (MCTD) رخ میدهد. MCTD با سطوح بالای آنتیبادیهای RNP بدون آنتیبادیهای Sm یا DNA دو رشتهای (dsDNA) مشخص میشود. MCTD شبیه LE است اما با درگیری کلیه همراه نیست.
آنتیبادیهای ریبونوکلئوپروتئین (RNP)، اغلب در سطوح بسیار بالا در بیماران مبتلا به انواع بیماریهای روماتیسمی سیستمیک از جمله روماتیسمی خودایمنی سیستمیک (SLE یا systemic lupus erythematosus )، اسکلروزسیستمیک پیشرونده، یک موجودیت بیماری متمایز با ویژگیهای بالینی متداخل SLE ، اسکلرودرمی، پلیمیوزیت و روماتیسم مفصلی دیده میشوند. این اتوآنتیبادیها معمولاً یک الگوی لکهدار قوی از رنگآمیزی هستهای در ایمونوفلورسانس ایجاد میکنند. ساختار آنتیژنهای شناسایی شده توسط آنتیبادیهای ضد RNP پیچیده است. رایجترین عوامل تعیین کننده و آنهایی که بهطور گسترده شناسایی میشوند، مواردی به نام RNP یا U1RNP هستند. آنتیبادیهای ضد RNP را میتوان بهتنهایی (معمولا در mixed connective tissue disease یا ( MCTD یا همراه با آنتی) Sm لوپوس) شناسایی کرد. Anti-Sm بهندرت بهتنهایی یافت میشود.
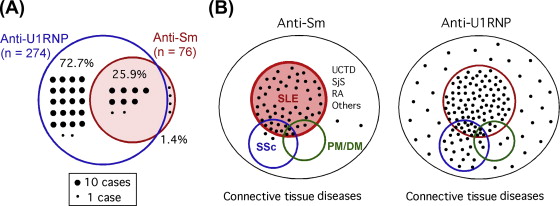
Autoantibodies
اوتوآنتیبادیها به ریبونوکلئوپروتئینهای هستهای کوچک (snRNPs) مانند anti-Sm و U1RNP جزو اولین پاسخهای پروتئین ضدهستهای بودند؛ که در بیماریهای روماتیسمی خودایمنی سیستمیک (systemic autoimmune rheumatic diseases یا SARD) شناسایی شدند. آنتیبادیهای Anti-Sm که U1، U2، U5 و U4-6snRNP ها را شناسایی میکنند، نشانگری برای لوپوس اریتماتوز سیستمیک ( SLEیا systemic lupus erythematosus) هستند، در حالیکه anti-U1snRNP را میتوان در SARD مختلف تشخیص داد، بیمارانی که دارای ویژگیهای همپوشانی SARD خاصی هستند که بهعنوان بافت همبند مخلوط نامیده میشود.
روشهای تشخیص ضد Sm و ضد RNP
روشهای تشخیص anti-Sm و anti-RNP در آزمایشگاههای مختلف متفاوت است و بر حساسیت، ویژگی و مقادیر پیشبینی تأثیر میگذارد. روشهای مورد استفاده شامل ایمونودیفیوژن، رادیوایمونواسی، ضدایمونوالکتروفورز (CIE)، هماگلوتیناسیون، یا سنجش ایمونوسوربنت مرتبط با آنزیم(ELISA) و وسترن بلات است. در بررسی ما، روش همیشه در بخش نتایج بیان شدهاست، زیرا ممکن است یک روش کاملاً با روش دیگری قابل مقایسه نباشد. علاوهبر این، هیچ یک از این روشها به خوبی بین آزمایشگاهها استاندارد نشدهاند.
تفسیر آزمایش
آنتیبادیهای RNP در سطوح بسیار بالایی در 95 تا 100 درصد بیماران مبتلا به بیماری بافت همبند مختلط یافت میشود. در واقع، اگر تیتر بالایی از RNP پیدا شود و سایر ویژگیهای ANA وجود نداشته باشد، مترادف با MCTD است. بحثهایی در مورد اینکه آیا MCTD نشاندهنده یک بیماری واقعاً متمایز است یا صرفاً یک سندرم همپوشانی وجود دارد. با این حال، سرولوژی تشخیصی واضح است حتی اگر دامنهی کامل درگیری بالینی در آن زمان مشخص نباشد. در سایر بیماریها، آنتیبادیهای ضدRNP اغلب با آنتیبادیهای پروتئینهای Sm مرتبط هستند. آنتیبادی ضد RNP و آنتیژن Sm در حدود 20 تا 30 درصد از بیماران مبتلا به SLE یافت میشود. 20-25 درصد بیماران مبتلا به اسکلروز سیستمیک پیشرونده دارای آنتی RNP هستند. آنها همچنین در سایر بیماریهای بافت همبند از جمله اقلیت کمتر از 1٪ از بیماران مبتلا به سندرم شوگرنس یا آرتریت روماتوئید یافت میشوند.
نتیجهگیری
آنتیبادی ضد Sm برای تشخیص SLE بسیار اختصاصی بوده و در افراد سالم یافت نمیشود و بهندرت در افراد مبتلا به سایر بیماریهای روماتیسمی یافت میشود. بنابراین، آزمایش آنتیبادی ضد Sm باید زمانی انجام شود که فرد به تشخیص SLE فکر میکند، اما نه برای کمک به تشخیص سایر بیماریهای روماتیسمی. آنتیبادیهای Anti-Sm با وجود بیماری کلیوی در بیماران مبتلا به SLE ارتباطی ندارد. این یافته منعکسکننده بیفایده بودن آنتیبادیهای ضد Sm بهعنوان پیشبینی کننده نفریت لوپوس (lupus nephritis) است. آنتیبادی ضد RNP مختص SLE نیست. اگرچه یک نتیجه آزمایش مثبت برای anti-RNP پشتیبانی بسیار قوی برای تشخیص MCTD ارائه می دهد، اما از تشخیص SLE، RA یا SSc پشتیبانی نمیکند. آزمایش ضد RNP برای تشخیص نفریت لوپوس ارزشی ندارد. مطالعات بیشتر برای نتیجهگیری معتبر در مورد ارتباط بین تست ضد RNP و سایر بیماریهای روماتیسمی، ظهور SLE و فعالیت بیماری ضروری است. آنتیبادیهای Anti-Sm و anti-RNP در مقایسه با سفیدپوستان، بیشتر در آمریکاییهای آفریقایی تبار یا آفریقایی-کارائیب دیده میشوند.
گردآوردنده: شعله جاهدی
منابع:
- https://emedicine.medscape.com/article/2086705-overview
- https://www.sciencedirect.com/science/article/pii/B978044456378100037X
- https://www.southtees.nhs.uk/services/pathology/tests/anti-rnp-antibody/
- https://neurology.testcatalog.org/show/RNP
- https://onlinelibrary.wiley.com/doi/full/10.1002/art.20836