
فهرست مطالب
ظهور فناوری پرینت سه بعدی در سالهای اخیر، محرک یک تغییر پارادایم در دنیای تولید و صنعت شده است. ادغام پرینت سه بعدی در مهندسی بافت، با استفاده از سلولهای زنده که در جوهرهای زیستی (مانند هیدروژلها) محصور شدهاند، راه را برای ابداع بسیاری از راهحلهای نوآورانه در زیست پزشکی و مراقبتهای بهداشتی هموار میکند. در این مقاله از بایوکن به قابلیتها، کاربردها و محدودیتهای فناوری چاپ زیستی سه بعدی میپردازیم.

فناوری چاپ زیستی سه بعدی
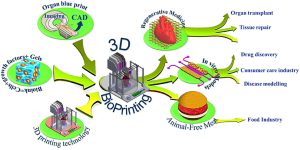
پرینت زیستی سه بعدی (3D Bioprinting) فرآیند یکپارچهسازی سلولهای زنده با مواد زیستی است. در این فرایند رسوب لایه به لایه و کنترل شدهی سلولها یا جوهر زیستی (Bioink)، تشکیل بافت زنده با ویژگیهای ساختاری و سلسله مراتبی مد نظر محققان را ممکن میسازد. پرینت زیستی سه بعدی از چندین فناوری مانند مهندسی بافت (tissue engineering)، زیستشناسی مصنوعی (synthetic biology) و توليد بيومتريال (biomaterial Production) بهره میبرد.
در شرایط آزمایشگاهی، سلولها نمیتوانند خود را مانند بافت واقعی در داخل بدن مرتب کنند. تکنیکهای مختلفی با هدف تقلید ساختار و عملکرد بافت زنده مورد استفاده و توسعه قرار گرفتند، مانند ساخت داربست، کشت بافت، بیورآکتورها، خودآرایی ECM و غیره. با این حال، استراتژیهای مهندسی بافت کنونی فاقد قابلیت ساخت بافتهای کاملاً کاربردی هستند. چاپ سه بعدی و چاپ کاغذ معمولی، سه مولفه اساسی و مشترك دارند: فایل مدل سه بعدی که باید چاپ شود مشابه فایل متنی است كه به پرینتر میدهیم، رنگ زیستی (شامل سلول ها و سایر مواد فعال زیستی) مشابه جوهر است، و چاپگر سه بعدی مشابه پرینتری است که جوهر را روی یک بستر یا پلتفرم چاپ میگذارد.
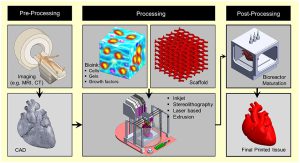
چاپ زیستی با به دست آوردن ساختار آناتومیکی بافت هدف با یک تکنیک تصویربرداری مناسب مانند توموگرافی کامپیوتری (CT) و تصویربرداری رزونانس مغناطیسی (MRI) شروع میشود. سپس از یک نرم افزار تخصصی برای ترجمه تصویر به نقشه CAD از لایههای مقطعی استفاده میشود تا دستگاه چاپ بتواند آنها را به صورت لایه به لایه اضافه کند. سپس، دستگاه چاپ زیستی بافت را با استفاده از یک روش چاپ خاص مانند چاپ زیستی جوهرافشان سه بعدی، چاپ زیستی سه بعدی میکرو اکستروژن، چاپ زیستی سه بعدی با کمک لیزر و لیتوگرافی استریو با استفاده از ترکیبی از مواد چاپی مانند داربست، جوهر زیستی و… میسازد. در نهایت، بافت ساخته شده به درون یک بیوراکتور منتقل میشود تا شرایط درون بدن برایش شبیهسازی شود و در آنجا دوره بلوغ حود را طی کند.
تکنیکهای چاپ زیستی سه بعدی
فناوری پرینت زیستی سهبعدی از چاپ دو بعدی سنتی روی کاغذ و بعداً چاپ سهبعدی مواد غیربیولوژیکی تکامل یافته است. بنابراین، جای تعجب نیست که جنبه مهندسی آن پیشرفتهتر از جنبه زیستی باشد. از آنجایی که این فناوری در ابتدا برای چاپ مواد غیر بیولوژیکی توسعه داده شده، در هنگام جایگزینی مواد ساختمانی با جوهرهای زیستی، مشکلاتی در زمینه سازگاری به وجود میآید. فارغ از تمام دغدغههای فنی، در اینجا فقط به طور خلاصه به تکنیکهای متداول چاپ سه بعدی زیستی میپردازیم:
- چاپ زیستی سه بعدی میکرواکستروژن (ریزترشحی): تکنیکی به کمک فشار است که معمولاً در چاپ مواد غیربیولوژیکی استفاده میشود. در فرآیند چاپ زیستی، جوهرهای زیستی انتخاب شده که در یک کارتریج شیشهای یا پلاستیکی ذخیره میشوند، معمولاً از طریق یک سرلوله (nozzle) با اعمال فشار پخش میشوند و توسط یک بازوی رباتیک کامپیوتری کنترل میشوند. جوهر زیستی به شکل یک رشته نازک از سرلوله خارج میشود و بر اساس طرح دیجیتال که موقعیت و مسیر حرکت سرلوله را تعیین میکند، شکل 3 بعدی مورد نظر برای بافت را میسازد. این تکنیک از پرینت سه بعدی مرسوم سرچشمه گرفته است و مشخص شده است که به دلیل یکپارچگی ساختاری، مناسبترین روش برای ایجاد سازههای در مقیاس بزرگ است. علاوه بر این می توان از انواع جوهرهای زیستی متنوع از جمله جوهرهای زیستی مبتنی بر داربست و بدون داربست با سرعت چاپ بالا استفاده کرد. با این حال، این تکنیک دارای دقت پایینی (تقریبا 100 میکرومتر) دارد؛ همچنین ممکن است فشار اکستروژن (ترشح) سلولهای زندهی درون جوهر زیستی را از بین ببرد.
- پرینت زیستی سهبعدی جوهرافشان (Inkjet 3D bioprinting): یک تکنیک غیرتماسی است که از نیروهای حرارتی، پیزوالکتریک یا الکترومغناطیسی برای بیرون راندن قطرات جوهرزیستی و قرار دادن آن روی بستر استفاده میکند. این تکنیک از چاپ معمولی و مبتنی بر کاغذ نشات گرفته است که آن را به یک رویکرد کمهزینه تبدیل میکند. دیگر مزایای چاپ زیستی جوهر افشان شامل چاپ با سرعت بالا و به کمک سرلولههای متعدد است، که باعث سالم ماندن سلولها در فرایند چاپ میشود. نقطه ضعف این روش نیاز آن به جوهر زیستی با ویسکوزیته کم است، چاپ هیدروژلهای غلیظ با این روش به سهولت انجام نمیشود.
- چاپ زیستی مبتنی بر استریولیتوگرافی (SLB): از پلیمر مایع قابل فوتوپلیمریزاسیون استفاده میکند که در آن نور UV یا لیزر در یک الگوی از پیش طراحی شده روی پلیمر هدایت میشود که منجر به اتصال عرضی و سخت شدن پلیمرها میشود. در هر چرخه پلیمریزاسیون، یک لایه نازک از ساختار ایجاد میشود و این چرخه پلیمریزاسیون برای تشکیل ساختار سه بعدی به صورت لایه به لایه، تکرار میشود. مزیت اصلی این فناوری در دقت بالای آن و عدم تنش برشی شدید نسبت به سایر تکنیکها است. با این حال، سلولها در معرض اشعه UV شدید برای اتصال متقابل قرار میگیرند که میتواند باعث آسیب سلولی شود.
کاربردهای پرینت زیستی سه بعدی
فناوری پرینت زیستی سه بعدی با بهرهگیری از موفقیت فوقالعاده چاپ نمونههای اولیه صنعتی در پروتزها و ابزارهای جراحی، کارآمد بودن خود را به خوبی ثابت کرد. گام بعدی در استفاده بهینه از پتانسیل این فناوری، تلاش برای ساختن بافتها و اندامهای زنده است. در ادامه به چند نمونه از تلاشهای انجام شده در این زمینه اشاره خواهیم کرد.
بیوپرینت سه بعدی برای پیوند اعضا
علیرغم محدودیتهای فنی و بیولوژیکی، چاپ زیستی در ساختن اندامهای کامل با آرایش سلسله مراتبی درست سلولها و بلوکهای بافتی در یک ریزمحیط سهبعدی نویدبخش است. برای چاپ بافتهای زنده، سلولها از سلولهای بنیادی بیمار یا یک اهداکننده گرفته میشوند و درون یک جوهرزیستی کشت داده میشوند. این مواد از طریق یک ژل یا داربست در کنار هم نگه داشته میشوند که میتواند سلولها را پشتیبانی کند و آنها را به شکل دلخواه درآورد تا عملکرد مورد نظر را به دست آورند.
فناوری تصویربرداری پیشرفته کنونی، مانند CT، ایجاد مدلهای CAD دقیق برای چاپ سه بعدی را برای اطمینان از تناسب کامل با بافت مورد نظر امکانپذیر کرده است. اخیراً چندین نمونه موفق در چاپ زیستی بافت سه بعدی برای ایجاد ساختارهای سطح اندامهابی چون استخوان، قرنیه، غضروف، قلب و پوست گزارش شده است.
بیوپرینت سه بعدی مدلهای اندام برای کشف دارو
تمرکز کنونی جامعه تحقیقات پزشکی، تمرکز بیشتر بر عوامل و شرایط پیچیده انسانی به جای تکیه بر مدلهای حیوانی است. مدلهای ساده آزمایشگاهی با تمام مزایایی که دارند از شبیهسازی پیچیدگیهای بدن انسان ناتوان هستند که این موضوع باعث ایجاد شکاف بزرگی بین مدلهای آزمایشگاهی و صنعت میشود.
به طور معمول، چاپ یک ارگان کارآمد به تعداد زیادی سلول از انواع مختلف نیاز دارد تا جایگزین عملکرد فیزیولوژیکی اندام آسیبدیده درون بدن شود. این موضوع تولید اندامهای زنده در مقیاس بالا را مشکل میکند. علاوه بر این، بدون تشکیل عروق خونی و لنفی، زنده ماندن اندام در طولانی مدت ممکن نیست؛ زیرا به دلیل انتشار محدود مواد غذایی و اکسیژن عملکرد اندام مختل میشود
ادغام چاپ زیستی و فناوری میکروسیال فرصتی عالی برای ایجاد مدلهای بافتی کوچک شده در شرایط آزمایشگاهی است. این تکنیک که با نام «ارگان روی تراشه» شناخته میشود، بر محدودیتهای ذکر شده غلبه میکند. به طور کلی پذیرفته شده است که مدلهای سه بعدی بافت در مقایسه با مدلهای دوبعدی بهتر و دقیقتر هستند. علاوه بر این، مدلهای بافتی مشمول سختگیریهای اخلاقی آزمایشهای بالینی نمیشوند.
چاپ زیستی سه بعدی برای گوشت بدون حیوانات
پروتئینهای حیوانی 40 درصد از کل پروتئین مصرفی جهانی را تشکیل میدهند. در حالی که انتظار میرود تقاضا برای پروتئین حیوانی تا سال 2050 به دلیل افزایش جمعیت جهان دو برابر شود، تولید فعلی دام با مشکلات متعددی مانند آلودگی، کوچک شدن زیستگاه حیوانات، افزایش فرسایش خاک و انتشار گازهای گلخانهای مواجه است. یکی از راه حلهای پیشنهادی برای رفع این مشکل، حرکت به سمت منابع گوشتی پایدارتر مانند تولید گوشت در شرایط آزمایشگاهی (IVM) است.
گوشت خوراکی عمدتاً از ماهیچههای اسکلتی همراه با سلولهای چربی، فیبروبلاستها و اندوتلیال تشکیل شده است که به آن ارزش غذایی میبخشد. تکنیک تولید بافتهای عضلانی در شرایط آزمایشگاهی بر انواع سلولهای مختلف برای شروع تولید گوشت متکی است که امیدوارکنندهترین آنها سلولهای myosatellite هستند. یک نیاز کلیدی در مهندسی بافت، داربستی برای حمایت از تکثیر سلولی است. تکثیر میوبلاست به داربستی انعطافپذیر با سطح بزرگی نیاز دارد که در نهایت به راحتی از محصول گوشتی نهایی جدا شود. با بهینه کردن صنعت چاپ زیستی برای رسیدن به تولید گوشت بدون حیوان، مقدار زیادی از درد و رنجهای غیرضروری تحمیل شده بر حیوانات متوقف خواهد شد.
گوشت آزمایشگاهی چیست و چگونه تولید می شود؟
چالشها و محدودیتهای فناوری چاپ زیستی سه بعدی
علیرغم پیشرفتهای قابل توجه، فناوری چاپ زیستی هنوز با چندین چالش جدی مواجه است. بزرگترین چالش، توانایی چاپ یک شبکه عروقی درون اندامی است، از شریانها و سیاهرگها گرفته تا مویرگها، که بدون آن بافتها زنده نمیمانند. در داخل بدن، فاصله سلولها از مویرگ چیزی بین از 100-200 میکرومتر است. این فاصله همان حد انتشار اکسیژن است.
ساخت ارگانهای بزرگ با مصرف اکسیژن بالا، مانند قلب و کبد، به تامین اکسیژن کافی برای جلوگیری از کمبود مواد مغذی و نکروز بافت نیاز دارد. ساخت مویرگهای خون در حال حاضر محدود به دقت دستگاههای چاپ سه بعدی است، چیزی حدود 20 میکرومتر است. در حالی که مویرگ خون میتواند به کوچکی 3 میکرومتر باشد. چندین راه حل امیدوارکننده برای ایجاد عروق مورد نیاز مطرح شده است، مثل ترکیب عوامل شیمیایی رگزا در بیوجوهرها برای القای رشد عروق پس از چاپ بافت.
تامین سلول یکی دیگر از چالشهای بزرگ این فناوری است، زیرا چاپ بافت به تعداد زیادی سلول نیاز دارد. منبع سلولهای بنیادی امیدوارکنندهترین انتخاب خواهد بود زیرا چاپ زیستی بر تمایز سلولهای بنیادی در مراحل مختلف فرآیند تأثیر میگذارد. یکی دیگر از محدودیتهای فعلی پرینت زیستی سه بعدی، توان عملیاتی کم و هزینه بالا است.
نویسنده: سینا جعفری

یک نظر