فهرست مطالب
فناوری آنتی سنس چیست؟
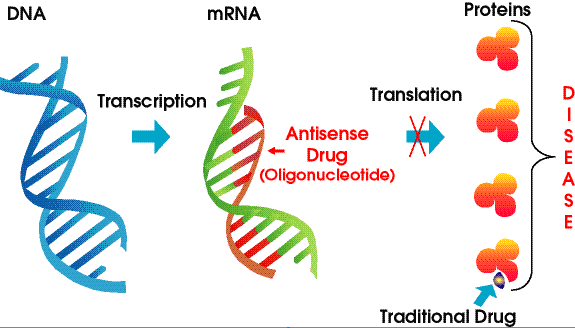
فناوری آنتی سنس یک رویکرد بیوتکنولوژیکی است؛ این فناوری که شامل استفاده از توالیهای اسید نوکلئیک مصنوعی برای هدف قرار دادن و تنظیم بیان ژنهای خاص در یک سلول است، هدف اولیه آن مهار انتخابی بیان یک ژن خاص با تداخل در فرآیند سنتز پروتئین است.
کاربرد فناوری آنتی سنس
فناوری آنتی سنس به دلیل توانایی آن در تنظیم انتخابی بیان ژنها، کاربردهای وسیعی، هم در تحقیقات و هم در درمان دارد؛ در ادامه به برخی از این کاربردها اشاره میکنیم:
- ژن درمانی
از فناوری آنتی سنس میتوان در ژن درمانی برای درمان اختلالات ژنتیکی مختلف استفاده کرد. هدف محققان با طراحی الیگونوکلئوتیدهای آنتی سنس (ASOs) برای هدف قرار دادن و مهار بیان ژنهای بیماریزا، اصلاح یا کاهش اثرات این اختلالات است.
به عنوان مثال، استفاده از ASO ها برای درمان بیماریهایی مانند دیستروفی عضلانی دوشن و فیبروز کیستیک مورد بررسی قرار گرفته است.
- درمان سرطان
فناوری آنتی سنس در درمان سرطان برای هدف قرار دادن و مهار ژنهایی که باعث رشد یا متاستاز سرطان میشوند مورد استفاده قرار میگیرد. با کاهش بیان این ژنها، ممکن است بتوان رشد تومور را کاهش داد و نتایج درمان را بهبود بخشید.
درمان ضد ویروسی
از ASO ها میتوان برای هدف قرار دادن ژنهای ویروسی استفاده کرد و آنها را به ابزاری بالقوه برای درمانهای ضد ویروسی تبدیل کرد. در زمینه عفونتهای ویروسی مانند HIV یا هپاتیت، ASOs میتواند با تکثیر ویروسی تداخل کند و بار ویروسی را کاهش دهد.
- اختلالات عصبی
استفاده از فناوری آنتی سنس برای درمان اختلالات عصبی در حال بررسی است. محققان در حال توسعه ASO برای هدف قرار دادن ژنهای خاص مرتبط با بیماریهایی مانند اسکلروز جانبی آمیوتروفیک (ALS)، بیماری هانتینگتون و آتروفی عضلانی نخاعی (SMA) هستند.
- بیماری های نادر
5ASO ها در درمان بیماریهای ژنتیکی نادر، که توسعه داروهای سنتی ممکن است از نظر اقتصادی امکان پذیر نباشد، بسیار امیدوار کنندهاند. آنها میتوانند برای رسیدگی به جهشهای ژنتیکی منحصر به فرد که بوجود آورنده این اختلالات هستند، مورد استفاده قرار گیرند.
- مطالعات عملکرد ژن
فناوری آنتی سنس ابزار ارزشمندی برای محققانی است که عملکرد ژن را مطالعه میکنند؛ با مهار انتخابی بیان ژنهای خاص، دانشمندان میتوانند نقش آن ژنها را در فرآیندهای سلولی و توسعه بیماری بررسی کنند.
- ژنومیک عملکردی
فناوری آنتی سنس را میتوان برای مطالعه سیستماتیک عملکرد همه ژنها در یک موجود زنده مورد استفاده قرار داد؛ زمینهای که به عنوان ژنومیک عملکردی شناخته میشود. این فرایند شامل استفاده از ASOs برای مهار یک به یک هر ژن و مشاهده تغییرات فنوتیپی ناشی از آن است.
- پزشکی شخصی
ASO ها را میتوان برای هدف قرار دادن ژنهایی با جهشهای خاص منحصر به فرد برای بیماری طراحی کرد. این رویکرد شخصی سازی شده، برای تطبیق درمانها با مشخصات ژنتیکی فرد است.
- بیماریهای التهابی
فناوری آنتی سنس به عنوان راهی برای تعدیل پاسخ ایمنی در شرایطی مانند آرتریت روماتوئید و بیماری التهابی روده با هدف قرار دادن ژنهای دخیل در التهاب، مورد بررسی قرار گرفته است.
- بیماری های قلبی عروقی
محققان در حال بررسی استفاده از ASO ها برای هدف قرار دادن ژنهای مرتبط با بیماریهای قلبی عروقی، مانند کلسترول بالا یا آترواسکلروز، برای کاهش خطر بیماریهای مرتبط با قلب هستند.
البته باید به این نکته توجه نمود که در حالی که فناوری آنتی سنس کاربردهای درمانی امیدوارکنندهای را در بر دارد، چالشهایی از جمله بهینهسازی روشهای استفاده از ASO، به حداقل رساندن اثرات جانبی و تضمین ایمنی در آزمایشات بالینی وجود دارد.
داروهای آنتی سنس
همانطور که اشاره کردیم، داروهای آنتی سنس دستهای از عوامل درمانی هستند که برای هدف قرار دادن و تعدیل بیان ژن خاص با استفاده از توالیهای اسید نوکلئیک مصنوعی به نام الیگونوکلئوتیدهای آنتی سنس (ASOs) طراحی شدهاند.
این داروها توانایی مهار انتخابی بیان ژنهای خاص در سطح مولکولی را دارند و این مسئله آنها را برای درمان انواع بیماریها، به ویژه آنهایی که دارای یک جزء ژنتیکی یا مبتنی بر RNA هستند، ارزشمند میسازند.
داروهای آنتی سنس با اتصال به توالیهای مکمل mRNA تولید شده توسط یک ژن هدف عمل میکنند. این اتصال میتواند به چندین پیامد منجر شود، از جمله مسدود کردن ترجمه mRNA به پروتئین، افزایش تجزیه mRNA و یا تغییر اتصال pre-mRNA، و در نهایت کاهش تولید پروتئین هدف.
انواع داروهای آنتی سنس
داروهای آنتیسنس شامل چندین نوع مولکول هستند که برای هدف قرار دادن و تنظیم بیان ژن طراحی شدهاند. این نوع از داروهای آنتی سنس بر اساس مکانیسمهای متفاوتی ساخته شدهاند.
- الیگونوکلئوتیدهای آنتی سنس “ASOs”
ASOها مولکولهای اسید نوکلئیک کوتاه، مصنوعی و تک رشتهای هستند که برای اتصال به توالیهای مکمل mRNA طراحی شدهاند.
این مولکولها میتوانند بیان ژن را با جلوگیری از ترجمه mRNA به یک پروتئین عملکردی مهار کنند. در ادامه به برخی از ASO ها اشاره میکنیم:
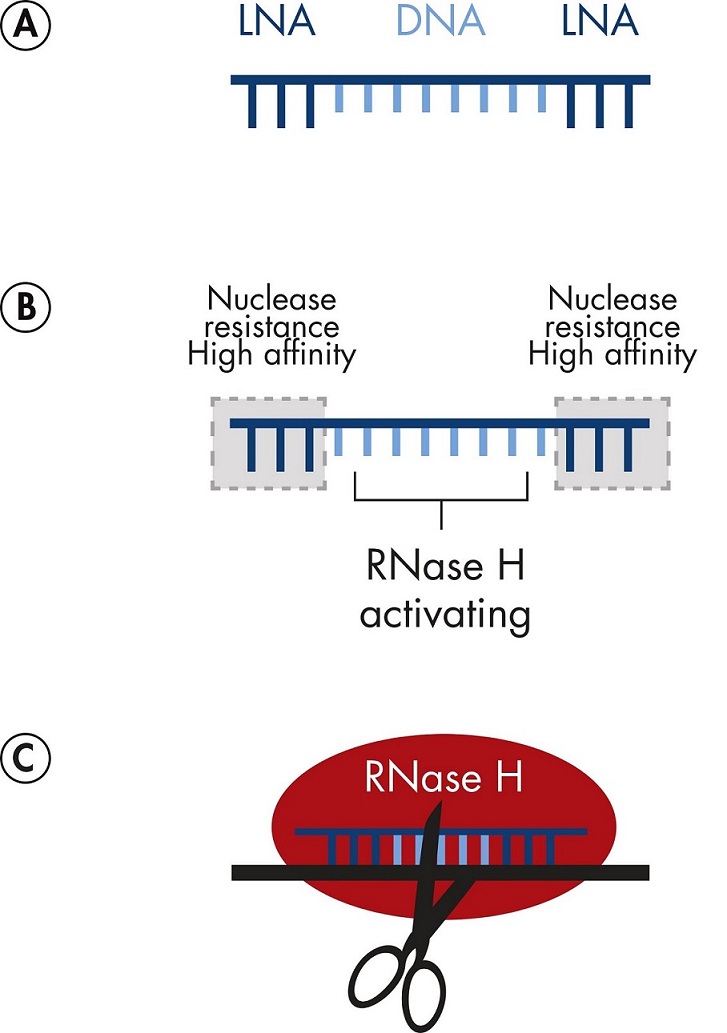
- ASO فسفروتیوات “Phosphorothioate ASOs”
این ASOها حاوی پیوندهای فسفروتیوات در ستون فقرات خود هستند که آنها را در برابر تخریب توسط نوکلئازها پایدارتر و مقاومتر میکند. از این نوع ASO ها میتوان به nusinersen (Spinraza) و eteplirsen (Exondys 51) اشاره کرد.
- 2′-O-Methoxyethyl (2′-MOE) ASOs
این مولکولها با تغییرات ایجاد شده در آنها، پایداری و میل اتصال آنها افزایش داده شده و از این دسته مولکولها میتوان به (Kynamro)mipomersen و اینوترسن (Tegsedi) اشاره کرد.
- Gammers
این مولکولها، ASOهایی هستند که طوری طراحی شدهاند این طراحی باعث افزایش تخریب mRNA هدف با واسطه RNAse H میشود.
- siRNA
مولکولهای SiRNA، مولکولهای RNA دو رشتهای هستند که میتوانند توالیهای mRNA خاصی را در یک سلول هدف قرار دهند. این مولکولها هنگامی که در داخل سلول قرار میگیرند، توسط کمپلکس خاموش کننده ناشی از RNA (RISC) پردازش میشوند تا mRNA هدف را تجزیه کنند و در نتیجه بیان ژن را مهار کنند.
داروهای مبتنی بر SiRNA برای بیماریهای مختلف، از جمله پاتیسیران (Onpattro) برای آمیلوئیدوز ارثی با واسطه ترانس تیرتین ساخته شده است.
- RNAi
تداخل RNA یک فرآیند سلولی طبیعی برای تنظیم بیان ژن است. محققان مولکولهای RNA مصنوعی را توسعه دادهاند که فرآیند طبیعی RNAi را تقلید میکند. این مولکولها را میتوان به سلولها رساند تا ژنهای خاص را بهطور انتخابی خاموش کنند.
داروهای مبتنی بر RNAi برای بیماریهای مختلف از جمله سرطان و عفونتهای ویروسی در حال بررسی هستند.
- آپتامرها “Aptamers”
آپتامرها مولکولهای کوتاه و تک رشتهای RNA یا DNA هستند که میتوانند به پروتئینهای هدف خاص با میل ترکیبی و اختصاصی بالا متصل شوند. آنها میتوانند در عملکرد پروتئین تداخل ایجاد کنند و منجر به اثرات درمانی شوند.
- ریبوزیمها “Ribozymes”
ریبوزیمها مولکولهای RNA با فعالیت کاتالیزوری هستند که میتوانند توالیهای خاص RNA از جمله mRNA را بشکنند. در حالی که از این روش کمتر از سایر روشهای آنتیسنس استفاده میشود، پتانسیل بالایی برای استفاده در حوزههای درمانی دارد و در دست بررسی است.
- سیستمهای CRISPR-Cas
اگرچه به طور کلی این سیستمها به عنوان داروهای آنتی سنس در نظر گرفته نمیشوند، میتوانند برای تنظیم ژن با هدف قرار دادن و ویرایش ژنهای خاص مورد استفاده قرار گیرند. درمانهای مبتنی بر CRISPR در زمینه درمان بیماریهای ژنتیکی بسیار امیدوارکنندهاند.
در نهایت، هر نوع داروی آنتی سنس مزایا و محدودیتهای خاص خود را دارد و انتخاب اینکه کدام یک از آنها استفاده شود بستگی به ژن هدف و بیماری خاص تحت درمان دارد.
داروهای آنتی سنس بر پایه RNA
داروهای آنتی سنس مبتنی بر RNA، که اغلب به عنوان درمانهای بر پایه RNA شناخته میشوند، از مولکولهای مختلف RNA برای هدف قرار دادن و تنظیم بیان ژن استفاده میکنند. تا اینجا به معرفی SiRNA، RNAi را مورد بررسی قرار دادیم؛ در ادامه به چند نمونه دیگر از درمانها و داروهای آنتی سنس بر پایه RNA اشاره میکنیم:
- ShRNA
RNA کوتاه سنجاق سری یا shRNA، مولکولهای RNA مصنوعی هستند که ساختار مولکولهای RNA طبیعی سنجاق سری را تقلید میکنند.این مولکولها را میتوان با استفاده از ناقلهای ویروسی یا پلاسمیدها، در داخل سلول بیان کرد، سپس، این مولکولها اغلب و به siRNA ها پردازش میشوند، که ژنهای خاص را هدف قرار داده و خاموش میکنند.
- MicroRNA
miRNA ها به طور طبیعی مولکولهای RNA کوچکی هستند که در تنظیم ژن نقش دارند. miRNA مصنوعی مشابه را میتوان برای تنظیم مثبت بیان ژن به سلولها وارد کرد، در حالی که از مهارکنندههای miRNA (آنتاگومیرها) میتوان برای کاهش بیان ژن از طریق مسدود کردن فعالیت miRNAهای درونزا استفاده کرد.
- lncRNA
برخی از داروهای آنتی سنس برای هدف قرار دادن RNA های طولانی غیر کد کننده یا lncRNAs طراحی شدهاند؛ این RNA ها، مولکولهایی هستند که پروتئین کد نمیکنند اما میتوانند نقشهای تنظیمی مهمی در بیان ژن ایفا کنند. با هدف قرار دادن lncRNA ها محققان در تلاشاند تا بر بیان ژنهای پایین دست و مسیرهای دخیل در بیماری تاثیر بگذارند.
داروهای آنتیسنس مبتنی بر RNA از دقت بالایی برخوردار هستند که آنها را برای درمان بیماریهای مختلف از جمله اختلالات ژنتیکی، عفونتهای ویروسی و سرطان مناسب میکند.
کاربرد داروهای آنتی سنس
داروهای آنتی سنس، از جمله داروهای آنتی سنس بر پایه RNA، به دلیل توانایی آنها در تنظیم انتخابی بیان ژن، کاربردهای وسیعی در هر دو حوزه تحقیقاتی و درمانی دارند. علاوه بر کاربرد در درمان سرطان، بیماریهای نادر، بیماریهای التهابی و خود ایمنی، بیماریهای قلبی عروقی، دارویهای آنتی سنس کاربرد های وسیع تری دارند که در ادامه به آنها اشاره میکنیم:
- درمان اختلالات ژنتیکی
داروهای آنتی سنس را میتوان برای هدف قرار دادن و درمان اختلالات ژنتیکی ناشی از جهشهای ژنی خاص یا بیان ژن نامنظم استفاده کرد. در ادامه به چند مورد از این اختلالات اشاره میکنیم:
- آتروفی عضلانی نخاعی “SMA”
(Spinraza) Nusinersen یک داروی آنتی سنس است که برای درمان SMA مورد استفاده قرار میگیرد؛ این بیماری یک اختلال ژنتیکی که با از دست دادن نورونهای حرکتی ایجاد میشود.
- دیستروفی عضلانی دوشن “DMD”
Eteplirsen (Exondys 51) داروی آنتی سنس دیگری است که برای درمان DMDمودر تایید قرار گرفته است. DMD یک بیماری ژنتیکی است که بر عملکرد عضلات تأثیر میگذارد.
- آمیلوئیدوز ارثی ناشی از ترانس تیرتین
پاتیسیران (Onpattro) و اینوترسن (Tegsedi) داروهای آنتی سنسی هستند که برای درمان این بیماری ژنتیکی نادر که با تجمع پروتئینهای غیرطبیعی ایجاد میشود، استفاده میشوند.
- درمان ضد ویروسی
داروهای آنتی سنس، به ویژه آنهایی که بر پایه RNA هستند، مانند RNAi یا siRNA ، میتوانند برای هدف قرار دادن و مهار تکثیر ویروسهای خاص طراحی شوند. این روش کاربردهای بسیاری در درمان عفونتهای ویروسی از جمله HIV، هپاتیت B و C و ویروسهای تنفسی دارد.
- اختلالات عصبی
داروهای آنتی سنس برای پتانسیل آنها در درمان اختلالات عصبی مانند بیماری آلزایمر، بیماری هانتینگتون و اسکلروز جانبی آمیوتروفیک (ALS) با هدف قرار دادن ژنهای دخیل در این بیماریها مورد استفاده قرار میگیرند.
- اختلالات متابولیک
این داروها میتوانند ژنهای درگیر در مسیرهای متابولیک را مورد هدف قرار دهند و درمانهای موثری را برای شرایطی مانند چربی خون یا سندرم متابولیک ارائه دهند.
- بیماری های چشمی
داروهای آنتی سنس برای درمان برخی بیماریهای چشمی، از جمله دژنراسیون ماکولا (AMD) مرتبط با سن و بیماریهای شبکیه در حال بررسی هستند.
داروهای آنتی سنس چگونه عمل میکنند؟
داروهای آنتی با هدف قرار دادن و تنظیم بیان ژن در سطح مولکولی کار میکنند. آنها از مولکولهای مصنوعی، مانند الیگونوکلئوتیدهای آنتی سنس (ASOs) یا درمان های بر پایه RNA، برای تداخل در تولید پروتئینهای خاص کدگذاری شده توسط ژنها استفاده میکنند.
- طراحی و سنتز داروهای آنتی سنس
محققان داروهای آنتی سنس را طوری طراحی می کنند تا مکمل mRNA تولید شده توسط ژن هدف باشند. این مولکولهای آنتی سنس معمولاً نسخههای کوتاهتر و مصنوعی RNA یا DNA هستند.
- تحویل داروهای آنتی سنس
داروهای آنتی سنس اغلب از طریق روشهایی مانند تزریق، به عنوان مثال، داخل وریدی یا تجویز خوراکی به بدن وارد میشوند. انتخاب روش تحویل دارو بستگی به پایداری دارو و بافت یا سلولهای هدف دارد.
- تشخیص هدف
هنگامی که دارو مورد نظر داخل سلول یا بافت هدف قرار میگیرد، مولکولهای دارویی آنتی سنس به دنبال mRNA مکمل ژن هدف میگردند.
- اتصال
مولکولهای دارویی آنتی سنس از طریق برهمکنشهای جفت باز به mRNA هدف متصل میشوند؛ توالیهای مکمل بین داروی آنتی سنس و mRNA این اتصال را امکان پذیر میکند. بسته به طراحی دارو، این اتصال میتواند به روشهای مختلفی رخ دهد:
- مهار ترجمه
برخی از داروهای آنتی سنس توانایی ریبوزوم را برای خواندن و ترجمه mRNA به پروتئین عملکردی را مسدود میکنند؛ این تداخل مانع از سنتز پروتئین میشود.
- تجزیه mRNA
سایر داروهای آنتی سنس باعث تخریب مولکول mRNA میشوند. این روش میتواند شامل به کارگیری آنزیمهای سلولی، به عنوان مثال RNAse H، برای جدا کردن mRNA باشد که منجر به تجزیه آن میشود.
- تغییر پیرایش
در موارد خاصی، داروهای آنتی سنس میتوانند بر روی پیوند pre-mRNA تأثیر بگذارند، که منجر به الگوهای پیوند جایگزین و تولید پروتئینهای غیرعملکردی یا کوتاه شده میشود.
- تنظیم بیان ژن
نتیجه اتصال داروی آنتی سنس به mRNA هدف، کاهش یا مهار بیان ژن مربوطه است. با کاهش سطوح mRNA، پروتئینهای عملکردی کمتری از آن ژن تولید میشود.
- اثرات درمانی
بسته به کاربرد خاص و مکانیسم اثر هر دارو، کاهش یا مهار بیان ژن میتواند اثرات درمانی خاص خود را داشته باشد.
- نظارت و بهینه سازی
نظارت بر اثربخشی و ایمنی درمان دارویی آنتی سنس ضروری است. محققان و تولیدکنندگان در این حوزه، تأثیر دارو بر بیان ژن و پاسخ بیمار به درمان را ارزیابی کرده و در صورت نیاز تغییراتی در آن انجام میدهند.
همانطور که گفته شد، داروهای آنتی سنس بسیار اختصاصی هستند و امکان هدف گیری دقیق ژنهای خاص را فراهم میکنند. این ویژگی یک مزیت بسیار مهم این روش است، زیرا میتواند عوارش جانبی را به حداقل برساند.
نویسنده: زهرا جهانبخش
تهیه شده در آکادمی بیوتکنولوژی ایران