فهرست مطالب
استخراج پلاسمید
پلاسمید یک دئوکسی ریبونوکلئیک اسید میباشد
که بهطور مستقل از DNA کروموزومی کپی میشود و امروزه در علم بیوتکنولوژی و مهندسی ژنتیک بهوفور استفاده میشود.
تاریخچه پلاسمید
اولین بار پلاسمید توسط Joshua Lederberg،
برنده جایزه نوبل شناسایی شد. پلاسمید یک دئوکسی ریبونوکلئیک اسید کوچک حلقوی خارج کروموزومی (DNA)
است که بهطور مستقل از DNA کروموزومی کپی میشود. اکثر میزبان پلاسمید، باکتری میباشد. پلاسمید در
زیستشناسی مولکولی، بیوشیمی، بیوتکنولوژی، زیست سلولی کاربرد گستردهای دارد. این بدان معنی است که خالصسازی/ جداسازی پلاسمید یک آزمایش اساسی در زمینههای تحقیقاتی
است و این آزمایش تقریباً در هر آزمایشگاه
روزانه انجام میشود. خاصیت شیمیایی پروتئین با اسیدهای نوکلئیک کاملاً متفاوت است. بنابراین، جدا کردن اسیدهای
نوکلئیک و پروتئینها نسبتاً آسان است. با این حال، RNA و DNA مولکولهای بسیار مشابهی با یکدیگر هستند.
در میان آنها، ریبوز موجود در RNA تنها از طریق ساختار گروهی از یک گروه هیدروکسیل (−OH) از دیاکسیریبوز
در DNA قابل تشخیص است. علاوه¬بر¬ این، DNA کروموزومی و DNA پلاسمید هر دو اسیدهای دیاکسیریبونوکلئیک هستند که دارای خواص شیمیایی یکسانی هستند.
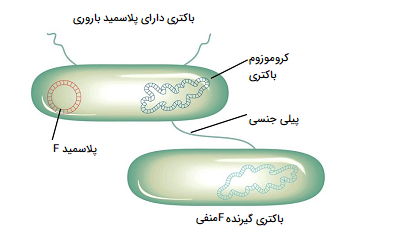
DNA پلاسمید
DNA کروموزومی و پلاسمید تقریباً در همه باکتریها به¬صورت دایرهای است. تفاوت قابل تشخیص آنها فقط اندازه
آنها است. DNA پلاسمید (۱۰ ~ جفت باز پایه) بسیار کوچکتر از DNA کروموزومی (برای مثال ۴.۶ میلیون جفت
باز در اشرشیاکلی) است. براساس این ویژگیها، تکنیک ویژهای برای استخراج DNA پلاسمید در بین این مولکولهای
زیستی مورد نیاز است. استخراج مستقیم DNA پلاسمید حاوی ژنهای مقاوم به آنتیبیوتیک از نمونههای پیچیده
هنگام مطالعه مقاومت آنتیبیوتیکی با واسطه پلاسمید از دیدگاه One Health ضروری است، تا نمای وسیعی از همه
پلاسمیدهای مقاومت موجود در این جوامع میکروبی به دست آید. همچنین تعداد کمی از گونههای باکتریایی
از محیطهای طبیعی وجود دارد که میتوانند در شرایط آزمایشگاهی کشت داده شوند. استخراج پلاسمیدها
از بخش قابل کشت این میکروبیومهای پیچیده ممکن است تنها نماینده کسری از کل پلاسمیدهای مقاومت آنتی
بیوتیکی موجود باشد.
افزایش سریع مقاومت آنتی¬بیوتیکی سبب مطالعات بیشتر در مورد عناصر ژنتیکی متحرک شدهاست. نشان
داده شدهاست که پلاسمیدها ناقل اصلی اشتراک ژن در بین باکتریها هستند و بنابراین نقش کلیدی در تکامل میکروبی
و گسترش مقاومت آنتیبیوتیکی ایفا میکنند، که سبب افزایش باکتریهای بیماریزای مقاوم می¬شوند. پلاسمیدهای
باکتریایی به ژنهای مقاومت اجازه میدهند تا بین گونهها و بین حیوانات و انسانها به صورت افقی منتقل شوند.
این تحرک پلاسمیدهای مقاوم به آنتیبیوتیک است که بیشترین نگرانی را ایجاد میکند، زیرا احتمالاً رایجترین
مکانیسم انتشار ژنهای مقاومت است
و بسیاری از پلاسمیدها توانایی حرکت از غیر را دارند.
مطالعه پلاسمید
برای مطالعه پلاسمیدوم مقاومت آنتیبیوتیکی
جمعیت میکروبی، باید روشهای کارآمدی برای استخراج جمعیت پلاسمید مستقیماً از نمونه مورد بررسی وجود
داشته باشد. با این حال، پلاسمیدها تنها بخش کوچکی از کل DNA موجود در نمونههای پیچیده را تشکیل میدهند
و جزء قابل کشت نمونه حتی کوچکتر است. روشهای سنتی مبتنی بر فرهنگ برای کار با نمونههای حیوانی یا محیطی
بسیار ایدهآل نیستند زیرا تنها بخش کوچکی از این باکتریها را میتوان در محیط آزمایشگاهی کشت کرد. بنابراین، تنها با تکیه
بر روشهای مبتنی بر فرهنگ، بخش بزرگی از پلاسمیدهای موجود در چنین نمونههایی از بین میروند. علاوه¬بر این،
استفاده از روشهای توالییابی بر اساس متاژنومیکها نیز محدودیتهایی دارد. عمق تعیین توالی معمولاً برای استخراج
کل پلاسمیدها از دادهها کافی نیست، مونتاژ به دلیل اندازه کوچک قطعات دشوار است و ژنهای موجود در مقادیر
کم از دست میرود. همچنین، پلاسمیدها اغلب حاوی توالیهای تکراری هستند که با DNA ژنومی به اشتراک گذاشته میشوند و
جمعآوری دادهها کوتاه خواندن را دشوار میکند.
بنابراین، باید مشخص شود که چه روشهایی قادر به استخراج این پلاسمیدهای مقاومتی بهطور مستقیم از نمونههای
پیچیده هستند و کدام یک نمای وسیعی از جمعیت پلاسمیدهای مقاوم به آنتیبیوتیک موجود در محیط میکروبی را ارائه میدهند.
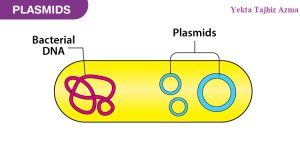
استخراج DNA پلاسمید
در حال حاضر، هیچ کیت برای استخراج DNA پلاسمید مستقیم از نمونههای پیچیده وجود ندارد. کیتهای
استخراج پلاسمید فعلی برای کار با کشت خالص باکتریایی در نظر گرفته شدهاست، که هنگام برخورد با نمونههای
پیچیده محیطی ایده¬آل نیست. کیتهایی که برای استفاده با نمونههای پیچیده مانند خاک یا مدفوع طراحی شدهاند
فقط DNA ژنومی را هدف قرار میدهند. لیز قلیایی یک روش پرکاربرد برای استخراج DNA پلاسمید با جداسازی
آن از DNA کروموزومی بر¬اساس اندازه کوچک و ماهیت فوق پیچیده پلاسمیدها است. با این حال، این فقط برای
استفاده در کشت باکتریایی در نظر گرفته
شدهاست، نه با نمونههای پیچیده که حاوی مواد دیگر و همچنین باکتریها هستند.
جداسازی پلاسمید برون¬زا
جداسازی پلاسمید برون¬زا با گرفتن پلاسمیدها
بهطور مستقیم از نمونه پیچیده در جفتگیریهای دو زایشی با استفاده از یک باکتری گیرنده عمل میکند. در حالی که
این روش اجازه میدهد تا پلاسمیدها به-طور مستقیم از نمونه بهدست آیند، اما به شدت به حفظ پلاسمید در
میزبان و توانایی پیوندی پلاسمیدهای موجود
در نمونه متکی است. بنابراین، این روش ممکن است بیان کلی از پلاسمیدهای موجود در نمونه را ارائه
ندهد، زیرا ممکن است بخش غیر همزمانی با این روش استخراج نشود. با این حال، پلاسمیدها می توانند توسط یک پلاسمید
خود انتقال¬پذیر بسیج شوند و بنابراین میتوانند با این روش نیز جذب شوند. علاوه¬بر این، روش برونزا میتواند
پلاسمیدهای خطی را که اغلب در محیطهای مختلف میکروبی یافت میشوند، جدا کند. روش برونزای جداسازی
پلاسمید بر اساس گرفتن پلاسمیدهای مزدوج به¬طور مستقیم از یک نمونه پیچیده، از طریق یک باکتری گیرنده در
جفتگیریهای دو زایمان است. این روش پلاسمیدهای مقاومتی با پروفیلهای متفاوت را به خود اختصاص داد
و همچنین سازگارترین روش بود و زمان¬بر نبود. معایب این روش این است که به تحرک پلاسمیدها در نمونه
اهداکننده متکی است و نمونه اهداکننده شامل یک شب فرهنگ کل جامعه باکتریایی است.
روش ضبط پلاسمید به کمک ترانسپوزون
ضبط پلاسمیدها به کمک ترانسپوزون (TRACA) به شما امکان میدهد پلاسمیدهای مقاوم به آنتیبیوتیک را
از نمونههای پیچیده به دست آورید. این روش با حذف هرگونه DNA کروموزومی آلوده از یک نمونه DNA کل،
و سپس قرار دادن ترانسپوزون بر روی پلاسمیدها با نشانگر انتخابی که شناخته شده¬است، کار میکند. پلاسمیدهای
خطی ممکن است با این روش اسیر نشوند، زیرا مبنای تکثیر Tn5 قادر به تکرار انتهای شدید آنها نیست و میتوانند
توسط اگزونوکلئاز تجزیه شوند مگر اینکه از آنزیمهای تخصصی استفاده شود. مزیت اصلی این روش این است که دارای
قابلیت جذب پلاسمیدهایی است که نشانگر قابل انتخاب برای E-COLI ندارند و ممکن است توانایی تکرار را
نداشته باشند. ذکر شدهاست که این روش بهنفع جداسازی پلاسمیدهای کوچک است، بنابراین ممکن است
تصوری نادرست از کل جمعیت پلاسمیدها ارائه دهد.
روش تقویت جابه¬جایی چندگانه
روش تقویت جابه¬جایی چندگانه با
حذف تمام DNA ژنومی بریده¬شده از یک نمونه DNA کل با DNase ایمن از پلاسمید کار میکند. باقی مانده DNA
پلاسمید دایرهای توسط DNA پلیمراز
phi29، که دارای مکانیسم دایره نورد است، تقویت میشود. به¬طور خلاصه، با استفاده از هگزامرهای
تصادفی، phi29 امکان تقویت غیراختصاصی DNA پلاسمید دایرهای موجود را فراهم میکند. فایده این
روش این است که حتی وقتی پلاسمیدها در تعداد بسیار کمی در مقایسه با کل DNA نمونه وجود دارند، این روش امکان تولید مقادیر زیادی DNA پلاسمید را میدهد. به¬طور مشابه، این
روش همچنین انتخاب پلاسمیدهای کوچک را ترجیح میدهد و مانند TRACA، پلاسمیدهای خطی را نادیده
میگیرد، که برخی از آنها ممکن است با درمان DNase تخریب شوند. همچنین باید توجه داشت که پلاسمیدهای
بزرگ میتوانند در طول استخراج بریده شوند، که ممکن است توسط تیمار اگزونوکلئاز نیز تخریب گردند.
نمونهها
نمونههای سرخ گوشتی از واحد تولید
مرغ تجاری در انگلستان جمعآوری شد. نمونهها لیوفیلیزه شدند و در دمای 80- درجه سانتیگراد ذخیره شدند. هر یک
از روشهای استخراج پلاسمید با همان نمونه سکوم انجام شد. همه روشها نیز با اشرشیاکلی NCTC 13400
حاوی پلاسمید pEK499 به عنوان شاهد انجام شد.
نتیجهگیری:
به¬تازگی، مطالعه پلاسمیدها شامل استخراج DNA پلاسمید است و به دنبال آن روشهای توالییابی گوناگون است.
با این حال، اگر پلاسمید های متعددی در یک نمونه وجود داشته باشند یا تعداد کپی آنها پایین باشد، بهدلیل عمق
فناوریهای توالی یابی متاژنومیکی فعلی، آنها از طریق تعیین توالی شناسایی نمیشوند. به¬طور مشابه،
مونتاژ با خواندن کوتاه دشوار است، بهخصوص اگر پلاسمیدها در تعداد کپی کم وجود داشته باشند یا اگر
خوانده شده با DNA ژنومی مطابقت داشته باشد. به منظور انجام مطالعات روی جمعیت کلی پلاسمیدهای
مقاوم موجود در یک نمونه پیچیده، روش
استخراج DNA پلاسمید باید بهینه شود تا بهترین نمایش را تا حد ممکن از کل پلاسمیدهای مقاومت موجود نشان دهد.
در حال حاضر فقط تعداد کمی از باکتریهای
محیطی در آزمایشگاه قابل کشت هستند.
این بدان معنی است که تنها با استفاده از یک روش مبتنی بر فرهنگ، تعداد پلاسمیدهای جدا شده را تا حد زیادی
محدود میکند. بنابراین، نمایش نتایج حاصل از یک مطالعه وابسته به فرهنگ، نمای محدودی از پلاسمیدوم
مقاومت کلی را ارائه میدهد.

نویسنده: آناهیتا یعقوبیانی
یک نظر